In einem der vorherigen Beiträge befassten wir uns mit den Grundlagen der chemischen Reaktion und den Enzymen, sowie dem Adenosintriphosphat. An dieser Stelle wird es Zeit sich mit einigen konkreten chemischen Reaktionen in unserer Zelle zu befassen.
Wir haben gelernt, dass Kohlenhydrate, zu denen u. a. Zucker und Stärke gehören, unsere zentrale Energiequelle sind, auf der fast alle Stoffwechselprodukte beruhen. Doch wie schaffen es unsere Zellen aus diesen Kohlehydraten ihre Energie zu gewinnen?
Dies geschieht mittels der Zellatmung.
Wir haben gelernt, chemische Reaktionen durch eine Reaktionsgleichung darzustellen. Wie würde diese Reaktionsgleichung bei der Veratmung von Glucose ausschauen?
Die entsprechende Summenformel der Zellatmung lautet: C6H12O6 +6 O2 +6 H2O → 12 H2O +6 CO2.
Eine vereinfachte, verkürzte Formel reduziert die Anzahl der Wassermoleküle, da sie sich mathematisch rauskürzen lassen: C6H12O6 +6 O2 → 6 H2O +6 CO2. (vgl. Abb. 1)

Abb. 1: Zellatmung
Aus einem Molekül Glucose und 6 Molekülen Sauerstoff entstehen 6 Moleküle CO2 und 6 Moleküle Wasser. Eine chemische Reaktion muss im Gleichgewicht sein, das heißt auf Seiten der Ausgangsstoffe (Edukte) müssen genauso viele Atome zu finden sein, wie auf Seiten der Reaktionsprodukte. Bei der Zellatmung handelt sich um eine exotherme Reaktion, bei der Energie freigesetzt wird, die Reaktionsprodukte (CO2 und Wasser) haben also ein niedrigeres Energieniveau, als die Edukte (Glukose und Sauerstoff). Die frei gewordene Energie wird in Form von ATP gespeichert.
Bei der Zellatmung werden die organischen Stoffe – hier also die Glukose – oxidiert. Glucose gibt bei dieser Reaktion also Elektronen ab. Der Sauerstoff dient dabei als Oxidationsmittel, der die Elektronen aufnimmt (also einem Elektronenakzeptor entspricht) und zu Wasser reduziert wird. Bei einigen Bakterien kommt außerdem die anaerobe Atmung vor, bei der anstelle von Sauerstoff andere Stoffe, z. B. Nitrat (NO3–) bei der Nitratatmung oder Sulfat SO42− bei der Sulfatatmung, als Oxidationsmittel dienen.
Von der Atmung ist die Gärung zu unterscheiden. Hierbei werden Moleküle zur Energiegewinnung abgebaut ohne Einbeziehung externer Elektronenakzeptoren wie Sauerstoff (O2) oder Nitrat (NO3−)
Werden Moleküle abgebaut, um Energie zu erzeugen, spricht man von Katabolismus, während beim Anabolismus Moleküle unter Energieverbrauch synthetisiert werden.
Nun sollte man sich aber nicht vorstellen, dass man einfach nur ein Stück Zucker in die Zelle einzufügen braucht und wie durch ein Wunder entsteht dabei die Energie, die wir brauchen. Damit aus Glucose Energie gewonnen werden kann, braucht es mehrere Zwischenschritte, die durch Enzyme katalysiert werden.
Wir werden uns daher vornehmlich mit dem beschäftigten, was auf dem Reaktionspfeil geschieht.
Die Zellatmung umfasst folgende Teilprozesse:
- die Glykolyse,
- den Citratzyklus und
- die Endoxidation in der Atmungskette.
Glykolyse
Die Glykolyse ist der erste Teilschritt der Zellatmung und findet im Zellplasma statt. Dieser Prozess kann ohne Sauerstoff ablaufen, ist also anaerob. Hierbei wird aus einem Molekül Glucose zwei Moleküle Pyruvat hergestellt. Pyruvat ist das Anion (negativ geladenes Atom) der Brenztraubensäure und ist die Ausgangssubstanz für viele weitere Stoffwechselwege. Die Bildung von Pyruvat aus Glucose erfolgt in 10 Teilschritten (Abb. 2), die in zwei Phase zusammengefasst werden. Bei Phase 1 wird Energie in Form von ATP verbraucht, bei Phase 2 ATP gebildet. Wir schauen uns diese Prozesse näher an.
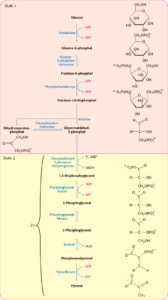
Abb. 2: Glykolyse
Phase 1.1.: Gelangt Zucker ins Zellplasma wird dieses mittels des Enzyms Hexokinase phosphoryliert und es entsteht Glucose-6-Phosphat. Phosphorylierung bedeutet, dass einem Molekül eine Phosphatgruppe angeheftet wird. Hierbei wird ein Molekül ATP verbraucht, welches dann zum ADP (Adenosindiphosphat) wird. Dieser Erste Schritt kostet also Energie, bezahlt wird mit einem ATP.
Phase 1.2.: Glucose-6-Phosphat wird dann in Fructose 6-Phosphat umgewandelt, dies wird durch das Enzym Glocose-6-Phosphat-Isomerase katalysiert.
Phase 1.3.: Der dritte Schritt kostet wieder Energie, es wird also mit einem Molekül ATP bezahlt: Aus Fructose-6-Phosphat wird Fructose-1,6-biphosphat. Das Enzym Phosphofructokinase katalysieret diesen Schritt. Wie der Name Fructose-1,6-biphosphat andeutet, hat dieses Molekül zwei Phosphatgruppen angeheftet, eines am 1. Kohlenstoffatom und die zweite am 6. Kohlenstoffatom.
Phase 1.4.: Mittels des Enzyms Aldolase wird die Fructose-1,6-biphosphat gespalten in zwei Molekülen mit je 3 Kohlenstoffatomen, sogenannte Triosephosphate. Einmal entsteht Glycerinaldehyd-3-phosphat und Dihydroxyacetonphosphat.
Phase 1.5.: Mittels des Enzyms Triosephosphat-Isomerase kann aus dem Dihydroxyacetonphosphat das Glycerinadlehyd-3-Phosphat gebildet werden. dieses gilt dann als Ausgangsstoff für die Phase 2 der Glykolyse.
Fassen wir eine Zwischenbilanz: in Phase 1 der Glykolyse wird aus einem Molekül Glukose zwei Moleküle Glycerinaldehyd-3-Phosphat gebildet. Diese Umwandlung kostet aber Energie in Form von zwei ATP. D. h. die Energiebilanz ist erstmal negativ. Die Energiegewinnung erfolgt über die Phase zwei. Hier sei erwähnt, dass Phase zwei doppelt abläuft. Wir haben ja nun zwei Moleküle Glycerinaldehyd-3-Phosphat
Phase 2.1.: Glycerinaldehyd-3-Phosphat wird über das Enzym Glycerinaldehyd-3-Phosphat-Dehydrogenase zu 1,3-Bisphosphogylcerat gebildet. Es kommt also eine zweite Phosphatgruppe hinzu. Diese Reaktion ist energetisch sehr günstig und hierfür wird anorganisches Phosphat genutzt (hier als Pi dargestellt), also welches, dass nicht an ATP gebunden ist. Bei dieser Reaktion tritt ein weiteres Molekül auf, dass bei chemischen Reaktionen in der Zelle äußert wichtig sein kann: das NAD+. NAD steht für Nicotinamid-Adenin-Dinukleotid und ist ein Coenzym und Oxidationsmittel und somit an zahlreichen Redoxreaktionen des Stoffwechsels der Zelle beteiligt. Es nimmt also Elektronen und wird zu NADH+H+ reduziert.
Phase 2.2.: 1,3-Bisphosphogylcerat hat nun zwei Phosphatgruppen. Mittels des Enzyms Phosphatgylceratkinase wird eine dieser Phosphatgruppen auf ein Molekül ADP übertragen und es entsteht ATP. Als Produkt entsteht 3-Phosphoglycerat. Da dieser Prozess ja doppelt abläuft entstehen zwei Moleküle ATP, womit die verbrauchten zwei ATP-Moleküle aus Phase 1 wieder „abbezahlt“ wurden. Die Energiebilanz liegt nun bei null.
Phase 2.3.: Aus 3-Phosphoglycerat wird über das Enzym Phosphoglycerat-Mutase 2-Phosphoglycerat. Bei diesem Schritt handelt es sich um eine einfache Umlagerung der Phosphatgruppe vom C3 zum C2-Atom.
Phase 2.4.: Aus 2-Phosphogylcerat wird über das Enzym Enolase Phosphoenolpyruvat. Dabei wird Wasser abgespalten.
Phase 2.5.: Im letzten Schritt der Glykolyse wird aus dem Phosphoenolpyruvat über das Enzym Pyruvatkinase die Phosphatgruppe auf ein Molekül ADP übertragen und es entsteht ATP. Als Produkt haben wir nun endlich das Pyruvat. Da auch dieser Prozess zwei Mal stattfindet entstehen zwei Moleküle ATP und damit haben wir eine positive Energiebilanz. Außerdem sind während der Phase 2 noch zwei Moleküle NADH+H+ entstanden, die später wichtig sein werden. Außerdem wurde pro Molekül Glucose 2 Moleküle Wasser abgespalten.
Fassen wir die Bilanz der Glykolyse zusammen:
Glucose + 2 NAD+ + 2 ADP + 2 Pi –> 2 Pyruvat + 2 NADH + 2 H+ + 2 ATP + 2 H2O
Gärung und Gluconeogenese
Das Endprodukt der Glykolyse ist Pyruvat, das aufgrund seiner vielseitigen Verwendbarkeit im Stoffwechsel eine zentrale Position einnimmt. Steht kein Sauerstoff zur Verfügung, kann Pyruvat in verschiedenen Gärungen verwendet werden. Am bekanntesten ist die alkoholische Gärung, wozu manche Mikroorganismen, z. B. Hefe, in der Lage sind bei dieser Reaktion wird keine Energie gewonnen, aber das Koenzym NAD+, der bei der Glykolyse verbraucht wurde, regeneriert (Abb. 3).
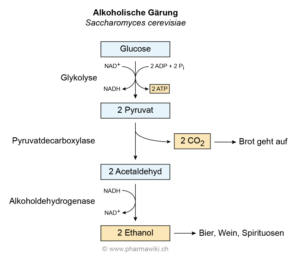
Abb. 3. Alkoholische Gärung
Die alkoholische Gärung verläuft in zwei Schritten. Im ersten Schritt wandelt die Pyruvatdecarboxylase das Pyruvat in Acetaldehyd um. Dabei wird CO2 abgespalten. Jeder der einen Hefeteig benutzt hat weiß das, denn durch diese Reaktion geht der Teig auf.
In Schritt zwei wird das Acetaldehyd über die Alkoholdehydrogenase in Ethanol umgewandelt und das ist der Alkohol der in unserem Bier, Wein oder Wodka drin ist. Dabei wird das NADH+H+ zu NAD+ regeneriert.
Andere Mikroorganismen nutzen andere Formen der Gärung. So können einige Bakterien aus Pyruvat Milchsäure herstellen. Dieser als Lactatgärung bezeichnete Prozess findet auch in unseren Muskeln statt, wenn beim Ausdauersport unsere Muskeln nicht mit genügend Sauerstoff versorgt werden.
Übrigens kann auch über die Gluconeogenese aus Pyruvat, aber auch aus anderen Molekülen wie Milchsäure, wieder Glucose hergestellt werden. Dieser Reaktionsweg wird immer dann eingeschlagen, wenn der Nachschub an Kohlehydraten gering ist (z. B. wenn man hungert). In manchen Fällen ist die Gluconeogenese eine Umkehrung der Glykolyse, weil z. B. dieselben Zwischenprodukte vorkommen und auch einige Enzyme in der Lage sind die Reaktion in beide Richtungen ablaufen zu lassen. Aber Glykolyse und Gluconeogenese unterscheiden sich durch vier Enzyme, sodass jeder Stoffwechselweg für sich reguliert wird und sich die beiden Reaktionswege nicht gegenseitig behindern. Des Weiteren findet die Gluconeogenese nicht im Zellplasma sondern in den Mitochondrien statt.
Mittels der Glykolyse kann Energie in Form von ATP gewonnen werden. Aber die Energiebilanz ist eher dürftig, denn unterm Strich bleiben zwei Moleküle ATP übrig. Beim Vorhandensein von Sauerstoff kann aber das Pyruvat weiter oxidiert werden und mehr ATP-Moleküle gewonnen werden. Der nächste Schritt ist nämlich der Citratzyklus.
Bei Citratzyklus, auch Krebszyklus oder Tricarbonsäurezyklus genannt, wird das Pyruvat weiter oxidiert. Der Citratzyklus findet nicht im Zellplasma, sondern in den Mitochondrien statt. Das Ausgangsmolekül dieses Reaktionsweges ist das Acetyl-Coenzym A, kurz AcetylCoA genannt. Dessen Bildung schauen wir uns genauer an
Oxidative Decarboxylierung von Pyruvat
Die Bildung von Acetyl-CoA ist ein mehrstufiger Prozess, welches in den Mitochondrien stattfindet und durch ein Multienzymkomplex katalysiert. Der Name dieses Multienzymkomplexes ist Pyruvatdehydrogenasekomplex (PDH-Komplex) und besteht aus drei Enzymen, die die wichtigen Teilschritte der Acetyl-CoA-Bildung katalysieren. Außerdem sind 5 Koenzyme beteiligt: Thiaminpyrophosphat (TPP), Liponsäure, FAD, Coenzym A und NAD+.
Es ist also eine recht komplexe Reaktion mit mehreren Zwischenschritten. Für uns wichtig ist aber folgendes (Abb.4):
Vom Pyruvat wird CO2 abgespalten wird und ein Acetyl-Rest entsteht. Der C3-Körper des Pyruvats wird also zum C2-Körper, weil nun ein CO2 abgespalten wurde. Dieser Acetyl-Rest wird oxidiert und es NAD+ wird zu NADH reduziert. Die Acetylgruppe wird auf das Coenzym A übertragen, sodass ein Molekül Acetly-CoA entsteht.
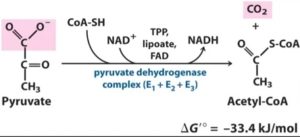
Abb. 4: Bildung von Acetyl-CoA
Acetyl-CoA dient als Brennstoff für den Citratzyklus in der nächsten Phase der Zellatmung. Die Bindung von CoA hilft dabei, die Acetylgruppe zu aktivieren und bereitet sie auf die notwendigen Reaktionen vor, um in den Citratzyklus einzutreten.
Citratzyklus
Der Citratzyklus ist ein zyklischer Stoffwechselprozess, der in den Mitochondrien stattfindet. Er wird gerne als die Drehscheibe des Stoffwechsels bezeichnet, da er eine zentrale Rolle für viele Stoffwechselwege einnimmt. So sind einige seiner Zwischenprodukte Ausgangsstoffe für die Synthese von Aminosäuren oder Fettsäuren. Sie werden dafür vom Citratzyklus für die entsprechenden Stoffwechselwege abgezweigt. Die wichtigste Funktion des Citratzyklus ist jedoch die Gewinnung von Elektronen (vor allem NADH) für die Atmungskette, also dem dritten Schritt der Zellatmung, durch das Oxidieren von Acetyl-CoA. Die einzelnen Reaktionsschritte des Citratzyklus werden in Abb. 5 dargestellt.
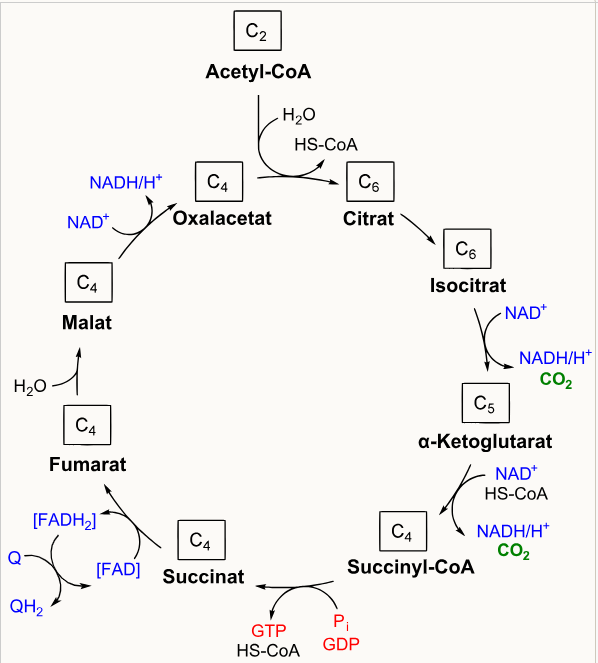
Abb. 5: Citrat-Zyklus
Hier finden sich 8 Schritte, die wir uns näher anschauen.
Schritt 1: Das Enzym Citratsynthase katalysiert die Übertragung von Acetyl-CoA auf Oxalacetat unter der Bildung von Citrat. Oxalacetat ist ein Molekül mit 4 Kohlenstoffatomen, Acetyl-CoA mit 2. Citrat ist somit ein Molekül mit 6 Kohlenstoffatomen. Bei dieser Reaktion wird H2O wird eingeführt und das Coenzym A abgespalten.
Schritt 2: Citrat wird durch das Enzym Aconitase zu Isocitrat umgewandelt. Dabei wird die OH-Gruppe des Citrats verschoben. Diese Reaktion kann problemlos in beide Richtungen verlaufen.
Schritt 3: Die Isocitratdehydrogenase katalysiert das Isocitrat zu α-Ketoglutarat. Dabei wird ein NAD+ zu NADH+H+ reduziert und es spaltet sich ein CO2-Molekül ab. In diesem Reaktionsschritt findet also die erste Oxidationsreaktion sowie die erste Decarboxylierung des Citratzyklus statt – mit Bildung von 1 NADH+H+ und Freisetzung von CO2.
Schritt 4: Die α-Ketoglutarat-Dehydrogenase ist ein großer Enzymkomplex, welcher sehr der Pyruvatdehydrogenase bei der Acetyl-CoA-Synthese ähnelt. Er benötigt für die oxidative Decarboxylierung von α-Ketoglutarat zu Succinyl-CoA folgende Cofaktoren: Thiaminpyrophosphat, Liponamid, Coenzym A, FAD und NAD+. Es entsteht erneut CO2 sowie 1 weiteres NADH+H+ für die Atmungskette.
Schritt 5: Aus Succinyl-CoA wird mittels des Enzyms Succinyl-CoA-Synthetase Succinat. Das Coenzym A wird abgespalten. Die dabei freiwerdende Energie wird genutzt um 1 GTP aus GDP zu synthetisieren – auch Substratkettenphosphorylierung genannt. GTP steht für Guanosintriphosphat und ist mit dem ATP verwandt. Überträgt man eine Phosphatgruppe des GTP auf ADP erhält man ATP: GTP + ADP → GDP + ATP. Diese Reaktion ist selbst jedoch kein Teil des Citratzyklus.
Schritt 6: Die FAD-abhängige Succinat-Dehydrogenase führt die Oxidation von Succinat zu Fumarat durch. Dies geschieht unter der Ausbildung einer Doppelbindung und Freisetzung von 1 FADH2. FAD steht für Flavin-Adenin-di-Nukleotid und ist ein Coenzym vergleichbar mit NAD+.
Schritt 7: Die Anlagerung von Wasser an Fumarat katalysiert die Fumarat-Hydratase – auch Fumarase genannt – und führt zur Ausbildung von Malat.
Schritt 8: Die NAD+-abhängige Malat-Dehydrogenase oxidiert Malat zu Oxalacetat, welches dann erneut als Substrat für Schritt 1 des Citratzyklus vorliegt. Hierbei entsteht 1 NADH+H+ für die Atmungskette.
Bilanz:
Bei der oxidativen Decarboxylierung dem dem Citratzyklus können folgende Bilanzen ermittelt werden:
Bilanz der oxidativen Decarboxylierung von Pyruvat:
2 Pyruvat + 2 NAD+ + 2CoA -> 2 Acetyl-CoA + 2 CO2 + 2 NADH + 2 H+
Bilanz des Citratzyklus:
2 Acetyl-CoA + 6 NAD+ + 2 FAD + 2 GPD + 2 Pi + 4 H2O -> 4 CO2 + 6 NADH + 6 H+ 2 FADH2 + 2 GTP + 2 CoA
Das entstandene CO2 ist unter diesem Gesichtspunkt lediglich ein Abfallprodukt zu verstehen. Für den nächsten Schritt, die Atmungskette, sind die 10 Moleküle NADH+H+ und 2 FADH2 Moleküle entscheidend.
Atmungskette
Im Citratzyklus werden überwiegend NADH+H+ und FADH2 produziert, die den Brennstoff für die Atmungskette und damit für die Synthese von ATP liefern. Man spricht auch von oxydativer Phosphorylierung. Die beiden reduzierten Coenzyme transportieren Elektronen, die bei der Oxidation von Pyruvat angefallen sind. Diese Elektronen werden für die Reduktion von Sauerstoff zu Wasser benötigt.
Hier heißt es durchatmen, denn die Atmungskette ist etwas schwerer nachzuvollziehen als die Glykolyse oder der Citratzyklus.
Die Atmungskette kann als Elektronentransportkette verstanden werden. Elektronentransportketten bestehen aus einer Reihe hintereinander geschalteter Redox-Moleküle, die in der Lage sind, Elektronen aufzunehmen bzw. abzugeben. Über diese Kette werden Elektronen von höheren Energieniveaus auf niedrigere weitergegeben, sie fallen sozusagen in Stufen bergab, wobei die einzelnen Redox-Moleküle ein zunehmend niedriges Energieniveau haben.
Die Enzyme der Atmungskette finden sich bei Eukaryoten (Zellen mit Zellkern) in der inneren Mitochondrienmembran, bei Prokaryoten (Zellen ohne Zellkern, wie Bakterien) in der Plasmamembran. Hier laufen zahlreiche Redoxreaktionen ab, also Reaktionen bei denen die Oxidation (Abgabe von Elektronen) einer Verbindung mit der Reduktion (Aufnahme von Elektronen) einer anderen Verbindung gekoppelt ist. In der Atmungskette werden die Elektronen von NADH+H+ und FADH2 schrittweise auf Sauerstoff übertragen, welcher dann zu Wasser reduziert wird.
Ein Mitochondrium ist ein von einer Doppelmembran umschlossenes Zellorganell, das eukaryotischen Zellen (d.h. Zellen, die einen Zellkern haben) zur Energiegewinnung dient (Abb. 6).
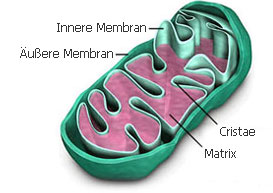
Abb. 6: Mitochondrium
Die äußere Membran grenzt das Mitochondrium nach außen ab und enthält Kanäle für die Durchlässigkeit von Molekülen. Die innere Membran bildet große Einfaltungen, die zisternenförmig das Innere des Mitochondriums ausfüllen (Cristae). In der Membran der Cristae befinden sich die Enzymkomplexe der Atmungskette und die ATP-Synthase, ein Transmembranprotein, dessen Funktion die Produktion von ATP ist.
Im inneren Membranraum findet sich die mitochondriale Matrix. In der Matrix findet man die ringförmige DNA des Mitochondriums und Ribosomen. Alle wesentlichen Enzyme des Citratzyklus sind im Matrixraum der Mitochondrien und daher in direkter Nachbarschaft der Atmungskette lokalisiert.
Abb. 7 zeigt die innere Mitochondrienmembran und ihre für die Atmungskette entscheidenden Bereiche.
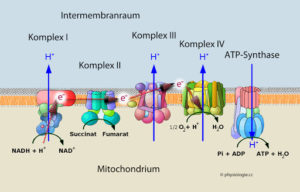
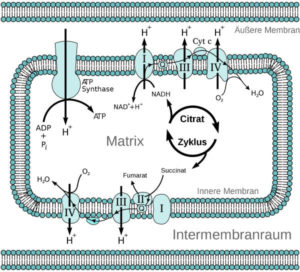
Abb.7: Atmungskette
Die mitochondriale Atmungskette besteht aus einer Reihe von Proteinkomplexen. Diese wirken als Oxireduktasen und werden als Komplex I-IV bezeichnet. Zusätzlich kommt die ATP-Synthase und die Wasserstoff- bzw. Elektronenüberträger Ubichinon (Coenzym Q) und Cytochrom c, die in die innere Mitochondrienmembran eingelagert sind, hinzu.
Die vier Komplexe der Atmungskette bestehen aus einer Reihe von Proteinen und enthalten Reaktionszentren mit Flavinen, Eisenschwefelkomplexen und Cytochrome, die die Übertragung der Wasserstoffe und Elektronen ermöglichen. Neben diesen dienen die Redoxhilfssubstrate Cytochrom und Ubichinon als Sammelbecken für Elektronen bzw. Wasserstoff. Zwischen den Proteinkomplexen finden Elektronenübergänge statt, die dabei freiwerdende Energie wird sofort zur Erzeugung bzw. Aufrechterhaltung des Protonengradienten umgesetzt.
Die aus dem Citratzyklus stammenden Coenzyme NADH+H+ und FADH2 geben Elektronen ab, die Protonen sammeln sich im Intermembranraum.
Die vier Komplexe der Atmungskette sind:
Komplex I: NADH-Dehydrogenase
Komplex II: Succinatdehydrogenase
Komplex III: Cytochrom-c-Reduktase
Komplex IV: Cytochrom-c-Oxidase
Über die Komplexe I, III und IV werden Protonen über die Membran gepumpt. Die Mehrzahl der Enzyme in diesen Komplexen, die die Elektronen weiter transportieren, verfügen über Eisenionen, die bei Elektronenaufnahme reduziert und bei Elektronenabgabe oxidiert werden. Da die Enzyme eine unterschiedliche Elektronegativität besitzen, werden die Elektronen von Enzym zu Enzym weitergegeben. Das nächstfolgende Enzym hat eine höhere Elektronegativität als das vorhergegangene. Es nimmt deshalb die Elektronen auf. Dadurch kann die Elektronentransportkette stattfinden.
Die Elektronentransportkette beginnt in der Mitochondrienmatrix mit NADH+H+, das Elektronen an Komplex I abgibt, also zu NAD+ oxidiert. Die Elektronen gelangen über Ubichinon zu Komplex III. Ubichinon ist in der Membran beweglich und steht in Kontakt mit Komplex II, der Elektronen von FADH2 erhält. Komplex III gibt Elektronen an Cytochrom c, dieses bindet an Komplex IV. Komplex IV reduziert letztlich den elementaren Sauerstoff, sodass Wasser entsteht 2 Elektronen werden auf ein halbes O2-Molekül übertragen, wobei Wasser (H2O) entsteht. Für die Arbeit des Komplexes IV ist Sauerstoff als finaler Elektronenakzeptor unersetzlich. Dies ist der Hauptgrund, warum Lebewesen Sauerstoff zum Leben brauchen.
Der Komplex II, die Succinatdehydrogenase, ist direkt an einer Reaktion des Citratzyklus beteiligt und schleust seine Elektronen von dort über enzymgebundenes FAD in die Atmungskette ein, übernimmt in der Atmungskette also keine Protonentransportfunktion.
Die Energie für die ATP-Synthese liegt im von der Elektronentransportkette erzeugten Protonen-Konzentrationsgefälle (sog. Chemiosmose), es entsteht also ein Konzentrationsunterschied (=chemisches Potential), in diesem Fall ein Protonengradient, da wir es mit H+ mit Protonen zu tun haben.
Die H+-Konzentrationen im Intermembranraum (hohe H+-Konzentration) und in der Mitochondrienmatrix (niedrige H+-Konzentration) unterscheiden sich stark. Damit haben wir auch einen unterschiedlichen pH-Wert. Zusätzlich entsteht ein Spannungsunterschied (elektrisches Potential), da durch die Verteilung der H+-Ionen der Intermembranraum positiver ist als die Mitochondrienmatrix (Abb. 8).
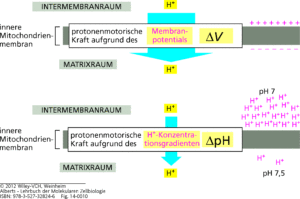
Abb. 8: elektrochemisches Potential
Der Gradient wird durch den Export von H+ von Komplex I, III und IV aufgebaut.
Biomembranen wie die Mitochondrienmembran bestehen aber aus einer Doppelschicht aus Phospholipiden und bilden dadurch eine Barriere für die geladenen Wasserstoffprotonen. Die H+-Ionen sind daher gefangen und können nicht frei durch die Membran diffundieren. Sie können nur durch ein Kanalprotein – die ATP-Synthase – diffundieren, um den Konzentrations- und Ladungsunterschied auszugleichen.
Das Enzym ATP-Synthase nutzt die Energie aus dem Gradienten und katalysiert beim Rücktransport der Protonen die ATP-Synthese. Das Enzym besteht aus einem Protonenkanal und einer zur Matrix gerichteten Kopfstruktur.
Der Protonenrückstrom erzeugt Energie. Das kann man sich wie bei einem Wasserkraftwerk vorstellen, bei dem Wasser hinter einer Staumauer angestaut wird. Dieser Rückstau wird verwendet, um die Turbinen zur Rotation zu bringen, um Strom zu generieren. Diese Turbine ist unserem Fall die ATP-Synthase. Sie koppelt die Diffusion der Protonen, wie ihr Name vermuten lässt, mit der Synthese von ATP aus ADP und einer Phosphatgruppe.
Nach Bindung von H+ findet eine Konformationsänderung statt, sodass das Proton in die Matrix abgegeben werden kann. Dabei rotiert die Kopfstruktur wie ein Rotationsmotor und erzeugt ATP-Moleküle.
Endbilanz
Glucose wurde somit zu den energiearmen Produkten CO2 und H2O abgebaut. Doch wie viel ATP entsteht bei der Atmungskette?
Bei der Oxidation eines NADH+H+ Moleküls aus dem Citratzyklus entstehen 2,5 Moleküle ATP. Die NADH+H+-Moleküle aus der Glykolyse befinden sich im Cytoplasma und müssen erstmal zu den Mitochondrien gebracht werden. Dies geschieht mittels Membranproteinen, die dieses NADH+H+ in den Intermembranraum der Mitochondrien transportieren, so z. B. das Glycerin-3-phosphat-Shuttle. Dadurch ist die Ausbeute von ATP in diesem Fall geringer, etwa 1,5 Moleküle ATP pro NADH+H+ aus der Glykolyse.
Wird jedoch das NADH + H+ der Glykolyse durch den Malat-Aspartat-Shuttle, einem anderen Membranprotein, in die Matrix gebracht, können daraus 2,5 ATP erzeugt werden. Damit können maximal 10 × 2,5 = 25 ATP (2 NAHD+H+ aus Glykolyse + 8 aus dem Citratzyklus) erzeugt werden.
Mit dem FADH2 verläuft der Vorgang im Prinzip genauso, nur gibt FADH2 auf einem niedrigeren Energieniveau Elektronen ab, sodass pro FADH2 maximal 1,5 ATP entstehen können. Da zwei FADH2 oxidiert werden, entstehen dabei 3 ATP.
Die Protonen und die Elektronen des NADH+H+ und des FADH2 (insgesamt 24) werden zusammen mit 6 Molekülen O2, die durch die Membran in die Mitochondrienmatrix transportiert werden, zu 12 H2O oxidiert.
Bilanz der Atmungskette (bei maximaler ATP-Ausbeute durch den Malat-Aspartat-Shuttle:
10 NADH + 10 H+ + 2 FADH2 + 28 ADP + 28 Pi + 6 O2 -> 10 NAD+ + 2 FAD + 12 H2O + 28 ATP.
Damit können in der gesamten Zellatmung bis zu 32 Moleküle ATP gebildet werden: 2 in der Glykolyse, 2 beim Citratzyklus (in Form von GTP) und 28 in der Atmungskette.
Da Prokaryoten keine Zellkompartimente besitzen, müssen sie nicht Energie für intrazelluläre Transportvorgänge ausgeben und können aus einer Glucose 36 bis 38 ATP gewinnen.


