Intro
Die Ordnung der Spechtvögel, die Piciformes, vereint einige der ungewöhnlichsten und am besten angepassten Vogelgruppen unseres Planeten: kraftvolle Spechte, tropische Tukane mit ihren überdimensionierten Schnäbeln – und die geheimnisvollen Honiganzeiger, die mit dem Menschen kooperieren, um an süße Beute zu gelangen.
Was sie verbindet, ist mehr als nur ein Name: spezialisierte Zungenapparate, ungewöhnliche Füße und interessante Schnäbel. Selbst Kreationisten sind von Spechten begeistert und sehen in ihrem komplizierten Zungenapparat ein Beleg für Gottes Schöpfung – die aber tatsächlich durch Evolution erklärt werden kann.
Insgesamt haben die Spechtvögel 9 Familien in zwei Unterordnungen: Die Glanzvogelartigen (Galbuloidea) mit den Faul- und Glanzvögeln und die Unterordnung der Spechtartigen (Picoidea) mit den Spechten, Honiganzeigern, Tukanen und vier Familien der sog. Bartvögel. Ein interessantes Merkmal, was diese Familien vereint ist der Bau ihrer Füße: sie sind zygodactyl: zwei Zehen zeigen nach vorne, zwei nach hinten.
Glanzvögel (Galbulidae)
Glanzvögel (Galbulidae) erinnern an Eisvögel, haben aber die für Spechtvögel typischen Flügel und zygodactylen Füße. Anders als die übrigen Spechtvögel können sie nicht gut klettern, da ihre Beine zu schwach und die Schwanzfedern nicht verstärkt sind. Der Schnabel ist lang und speerförmig und die schlitzförmigen Nasenöffnungen werden von Borsten bedeckt. Die Glanzvögel kommen in 18 Arten in 5 Gattungen in den Tropen Mittel- und Südamerikas vor. Die Schwanzfedern sind bei den meisten Arten fächerartig angeordnet, bei manchen aber auch übereinander zusammengelegt, wobei die zwei mittleren Federn über die äußeren hervorragen. Das Gefieder ist goldgrün und smaragdgrün glänzend, die Schwungfedern sind dunkel und die Brust und der Bauch von rosa bis rotbraun gefärbt. Der unbefiederte Ring um die Augen hat eine schmale Verbindung zum Schnabel. In sitzender Haltung schieben die Vögel ihre Brust weit vor und heben den Kopf leicht an. Die Körperlänge beträgt 15 bis 30 cm, ihr Gewicht 15 bis 25 Gramm. Alle Glanzvögel sind Einzelgänger und leben an Waldrändern, nur in der Fortpflanzungszeit kommen sie zusammen. Sie ernähren sich hauptsächlich von Insekten, einige Arten haben sich auf die Schmetterlingsgattung Morpho spezialisiert. Die Nisthöhle wird in Uferböschungen oder die Bauten von Termiten mit ihren Füßen gegraben (Winkler et al. 2015, 2025a, Del Hoyo et al. 2002, Del Hoyo 2020).
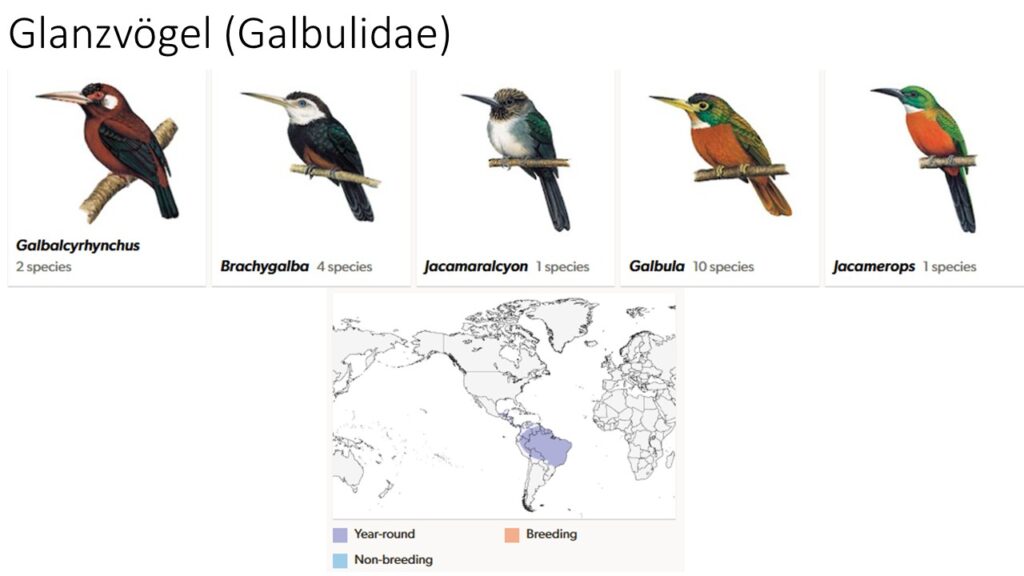
Faulvögel oder Tamatias (Bucconidae)
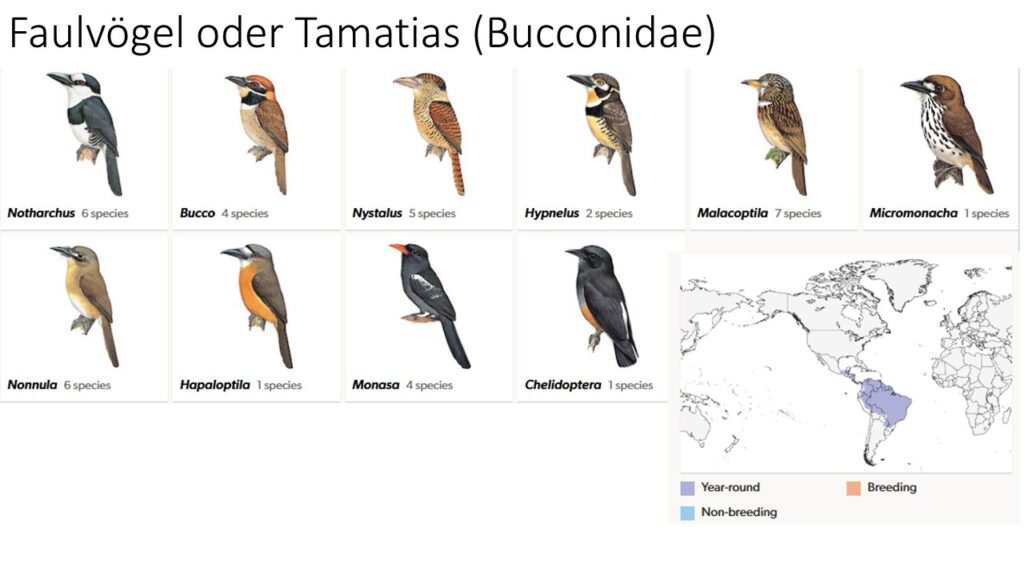
Faulvögel ähneln den Glanzvögeln, sind aber plumper, haben einen großen Kopf und einen kürzeren aber breiteren Schnabel. Die Vögel haben eine düstere, wenig kontrastreiche Gefiederfärbung. Faulvögel werden 16 bis 20 cm groß. 40 Arten in 12 Gattungen kommen in Mittel- und Südamerika vor, die meisten Arten im Amazonas-Regenwald (Winkler et al. 2015, 2025b, Del Hoyo et al. 2002, Del Hoyo 2020). Faulvögel sind überwiegend Einzelgänger, aber Vertreter der Gattung Monasa sind gesellige Vögel und helfen einander beim Brüten. Faulvögel sitzen oft regungslos auf Ästen, dies hat ihnen den deutschen Namen eingebracht. Ihr englischsprachiger Name „puffbird“ geht auf ihr flauschiges Gefieder zurück. In dieser sitzenden Haltung sonnen sie sich oder halten nach Insekten Ausschau, auf die sie sich herabstürzen und im Flug fangen. Auch sie brüten in Nisthöhlen, z. B. an Uferhängen oder Termitenbauten. Faulvögel geben kaum Laute von sich, sie gehören zu den leisesten Vögeln Südamerikas. Molekulare Untersuchungen ergaben, dass sich die Gattung Nonnula vor schätzungsweise 25 Millionen Jahren vom gemeinsamen Vorfahren der anderen Faulvögel abspalteten, wobei die Gattung Malacoptila vor etwa 19,1 Millionen Jahren die nächste Abspaltung darstellte (Witt 2004). Faul- und Glanzvögel sind bisher nicht fossil dokumentiert. Ursprünglich würde die Gattung Primobucco aus dem Eozän Wyomings anhand fragmentarischer Fossilüberlieferungen zuerst als Faulvogel klassifiziert. Spätere Untersuchungen, basierend auf vollständigeren Fossilbelegen, ordnen diesen aber in die Verwandtschaft der Rackenvögel (Mayr 2009, 2016, Brodkorb 1970, Ksepka & Clarke 2010).
Die Familie der Sylphornithidae, die im späten Eozän und frühen Oligozän Europas vorkamen und die Gattungen Sylphornis und Oligosylphe umfassen (Mourer-Chauviré 1988a; Mayr 2009a) weisen eine Reihe von Merkmalen auf, die an Spechtvögel erinnert. Es sind kleine Vögel mit einem langen und schlanken Tarsometatarsus. Sie hatten zumindest fakultativ zygodaktyle Füße, und ihr Carpometacarpus ähnelt ebenso den Spechtvögeln. Eine phylogenetische Analyse ergab, dass diese Vögel das Schwestertaxon entweder der Glanz- und Faulvögel oder aller anderen Spechtvögel sind (Mayr 2009, 2016, Duhamel et al. 2020).
Tukane (Ramphastidae)
Tukane gelten in unseren Breitengraden als die typischen Tropenvögel und wurden in der westlichen Welt als Werbefigur genutzt. In den 1930er und 40ern nutzte die Marke Guinnes einen Tukan als Werbefigur, Kellogs nutzt einen Tukan für seine Marke Froot Loops und Haribo für ihr Produkt Tropifrutti. Generell: viele Marken – ob Fruchtsäfte, Kosmetikprodukte oder Reiseanbieter nutzen, wenn sie nicht auf Papageien zurückgreifen, oft einen Tukan als Werbefigur, wenn etwas Tropisches verkauft werden soll. Und tatsächlich: Tukane sind, was ihr Aussehen betrifft, sehr imposante Vögel (Winkler et al. 2015, 2020a, Del Hoyo et al. 2002, Del Hoyo 2020).
Das auffälligste Merkmal ist der riesige, aber leichtgewichtige, am Rand gesägte und prächtig gefärbte Schnabel. Der wissenschaftliche Name der Tukane, Ramphastidae, heißt so viel wie „Großschnabel“. Er dient unter anderem der Kontrolle des Wärmehaushaltes, indem die Blutzufuhr zum Schnabel je nach Umgebungstemperatur kontrolliert wird. Die nicht isolierte Oberfläche des Schnabels wirkt bei hohen Außentemperaturen wie ein Kühlradiator, der überschüssige Körperwärme abführt (Tattersall et al. 2009).
Die enormen Schnäbel der Tukane sind darauf spezialisiert Früchte oder andere Nahrung zu fressen. Man geht jedoch davon aus, dass die spektakulären Farben der Schnäbel der Tukane in erster Linie der Anlockung von Partnern oder der Partnererkennung während der Balz dienen. Der Schnabel des Tukans hat sich also wahrscheinlich durch sexuelle Selektion (Selektion in direktem Zusammenhang mit dem Partnererwerb) sowie durch natürliche Selektion entwickelt.
Der Bau der Füße entspricht dem der anderen Spechtvögel. Die Tukane ernähren sich vorwiegend von Früchten, nehmen aber auch Insekten, Spinnentiere und sogar kleine Reptilien oder Säugetiere zu sich. Tukane leben monogam und nisten in Baumhöhlen. In Afrika und Asien wird die ökologische Rolle der Tukane von den Nashornvögeln übernommen.
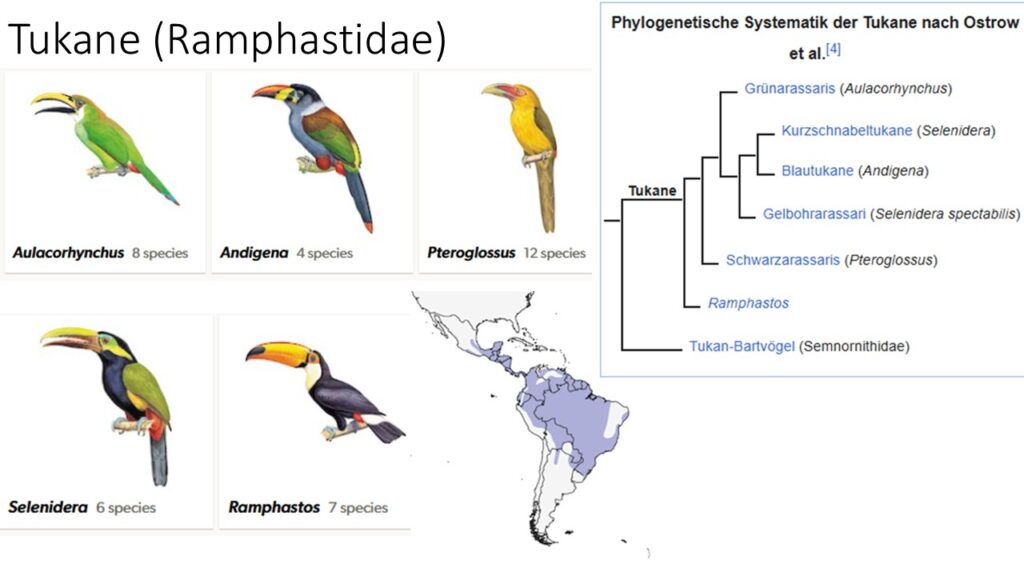
Es gibt 5 Gattungen der Tukane – die eigentlichen Tukane (Ramphastos), Grünarassaris (Aulacorhynchus), Blautukane (Andigena), Schwarzarassaris (Pteroglossus) und die Kurzschnabeltukane (Selenidera) – die Artenzahlen schwanken von 36-51 Arten, je nachdem ob einzelne Unterarten auf den Status einer Art erhoben werden. Sie alle kommen nur in Mittel- und Südamerika vor. Fast alle Arten bewohnen Regenwälder, lediglich der Riesentukan (Ramphastos toco), die vielleicht bekannteste Tukanart, kommt in halboffenem Gelände vor. Mit einer Körperlänge von bis zu 62 cm und einem Gewicht von 680 g ist er die größte Tukanart. Der Schriftarassari (Pteroglossus inscriptus), dessen Name sich aufgrund unregelmäßiger schwarzer Markierungen auf dem Schnabel ableitet, gehört mit 33 cm Körperlänge und 130 g Gewicht zu den kleinsten Arten der Tukane. Die Gattung der Blautukane (Andigena) hat ein beschränktes Verbreitungsgebiet und konzentriert sich auf die Bergwälder der tropischen Anden.
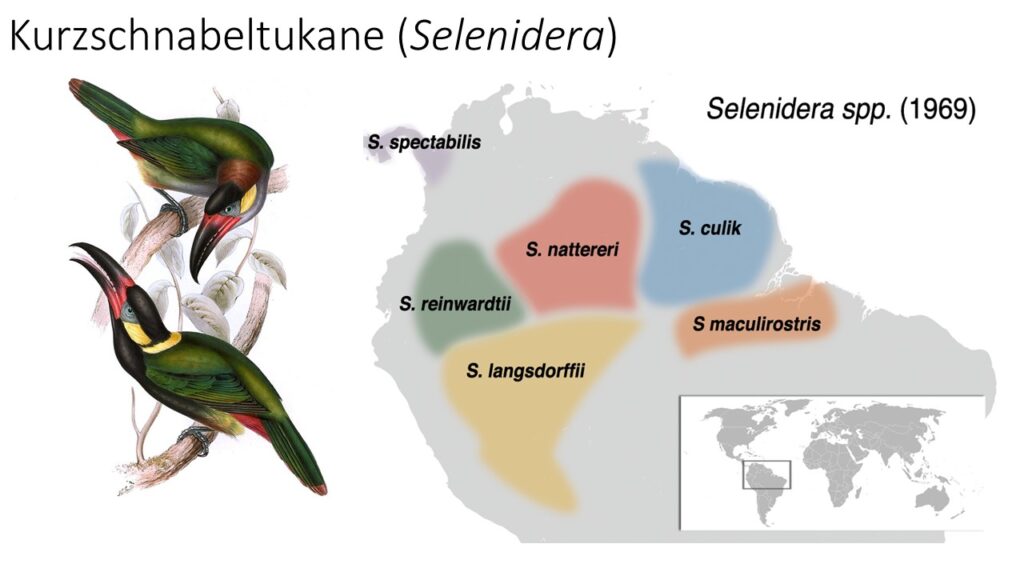
Das Gefieder weist bei vielen Arten knallig bunte Farben auf, die oft mit glänzend schwarzen Gefiederpartien kontrastieren. Die Geschlechter unterscheiden sich kaum, lediglich bei den Kurzschnabeltukanen (Selenidera) haben die Geschlechter eine unterschiedliche Färbung. Die Kurzschnabeltukane dienten auch als Modelle für die Entstehung neuer Arten. Nach Ansicht des deutschen Ornithologen Jürgen Haffer aus den 1960er Jahren stammen die rezenten Arten der Kurzschnabeltukane von einer Art ab, deren Verbreitungsgebiet fragmentiert wurde, als in den trockeneren Zeiträumen des Pleistozäns die Regenwälder schrumpften und nur noch in den feuchteren Regionen zu finden waren. In diesen voneinander isolierten Verbreitungsgebieten entwickelten sich die einzelnen Arten. Die Ausdehnung der Regenwälder in den feuchteren Zeiträumen des Pleistozäns führte dazu, dass die Verbreitungsgebiete der einzelnen Arten wieder größer wurden und heute stellenweise aneinandergrenzen (Haffer 1969).
Die Refugien-Hypothese Haffers ist nicht unumstritten. Hauptkritikpunkt ist, dass es wenige empirische Daten gibt, die diese belegen. Sie gilt aber als ein möglicher Erklärungsansatz für den Artenreichtum Südamerikas. Für die Theorie spricht, dass die jeweiligen Verbreitungsgebiete jeweils ein Flusssystem als Zentrum haben. Im vorliegenden Fall der Kurzschnabeltukane dürfte die Refugienhypothese jedoch zutreffen, da sich die Verbreitung der Arten auf die großen Flusssysteme konzentriert. Da Tukane relativ sesshafte Vögel sind, die kaum weite Strecken wandern können große Flüsse für diese Gruppe Isolationsbarrieren darstellen und die Bildung neuer Arten führen. Bei anderen Vogelgruppen trifft dies aufgrund besserer Flugleistung nicht unbedingt zu.
Bartvögel: vier Familien statt einer
Bartvögel verdanken ihren Namen der an der Schnabelbasis entspringenden steifen Borsten. Ursprünglich waren sie als eine Familie klassifiziert, aber molekularbiologische Untersuchungen zeigen, dass einige Bartvögel enger mit Tukanen verwandt sind als mit anderen Bartvögeln.
Deshalb werden die Bartvögel in vier Familien aufgeteilt: die in den Tropen Mittel- und Südamerikas vorkommenden Tukan-Bartvögel (Semnornithidae) und Amerikanischen Bartvögel (Capitonidae), die Afrikanischen Bartvögel (Lybiidae) und die Asiatischen Bartvögel (Megalaimidae). Alle Bartvögel und die Tukane bilden gemeinsam die Infraordnung Ramphastides. Viele Arten haben ein farbenprächtiges Gefieder. Sie ernähren sich von Insekten und Früchten und sind wie alle Spechtvögel Höhlenbrüter.
Die Tukanbartvögel oder Zinkenschnäbel (Semnornithidae) haben zwei Arten – Tukanbartvogel (Semnornis ramphastinus) und Azteken-Bartvogel (Semnornis frantzii) – in einer Gattung und sind mit den Tukanen näher verwandt als mit den Amerikanischen Bartvögeln. Sie sind verhältnismäßig große Bartvögel und werden 18-22 cm lang. Der Azteken-Bartvogel, der die Bergwälder von Costa Rica und Panama bewohnt, ist insgesamt eher olivgrünlich mit einer matt orangebraunen Brust. Der Tukan-Bartvogel, der in den Bergwäldern Ecuadors und Kolumbiens lebt, ist dagegen deutlich farbenprächtiger und zeichnet sich durch einen schwarzen Oberkopf, eine hellgraue Kehle, eine leuchtend rote Brust sowie einen kräftig goldorangen Bürzel und Flanken aus (Winkler et al. 2015, 2020b, Del Hoyo et al. 2002, Del Hoyo 2020, Ostrow et al. 2023).

Die Amerikanischen Bartvögel (Capitonidae) kommen in 15-18 Arten in zwei Gattungen in den Regenwäldern Mittel- und Südamerikas vor. Sie sind in der Regel sehr bunt und zeigen grüne, rote, gelbe, weiße oder schwarze Tönungen. Dabei sind Männchen in der Regel farbiger als die Weibchen. Amerikanische Bartvögel werden 15 bis 20 Zentimeter lang. Der Rumpf ist kurz, der Hals kurz und dick und der Kopf kann im Verhältnis zum Körper relativ groß sein. Der Schnabel ist kurz und dick und weist an den Kanten oft eine Sägung auf. Im Vergleich zu anderen Bartvögeln besitzen Amerikanische Bartvögel nur wenige und kurze Borsten an der Schnabelbasis. Die Rufe der Amerikanischen Bartvögel ähneln denen kleiner Eulen (Winkler et al. 2015, 2020c, Del Hoyo et al. 2002, Del Hoyo 2020).

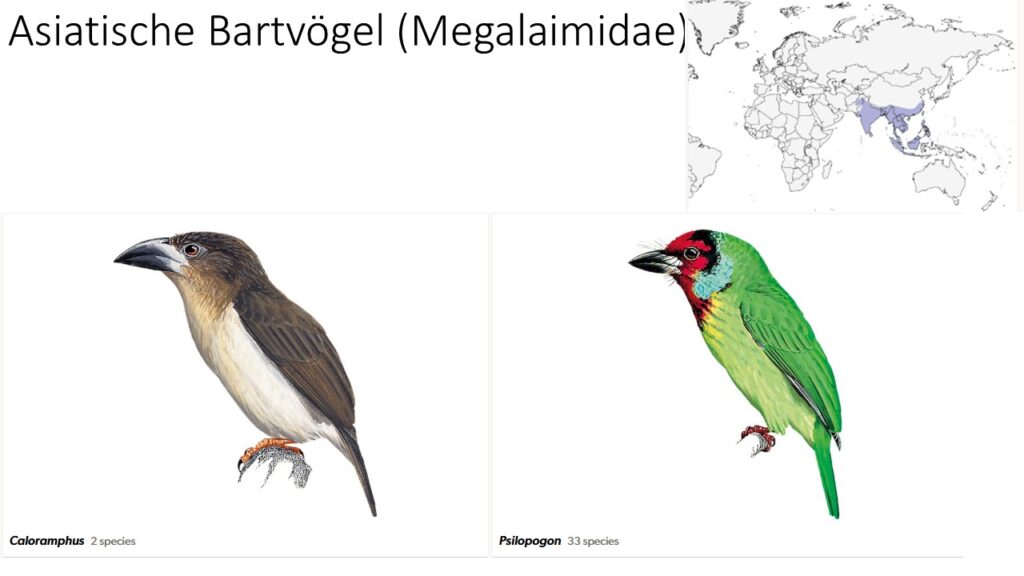
Die Asiatischen Bartvögel (Megalaimidae) leben mit 35 Arten in 2 Gattungen in den Wäldern des tropischen Asiens. Während die 2 Arten der Gattung Calorhamphus bräunlich gefärbt sind, dominieren bei der Gattung Psilopogon Grüntöne. Beide Gattungen trennten sich vor etwa 21 Mio. Jahren und werden von manchen auch als zwei Unterfamilien anerkannt (Winkler et al. 2015, 2020d, Del Hoyo et al. 2002, Del Hoyo 2020, den Tex & Leonard 2013, David 2008).
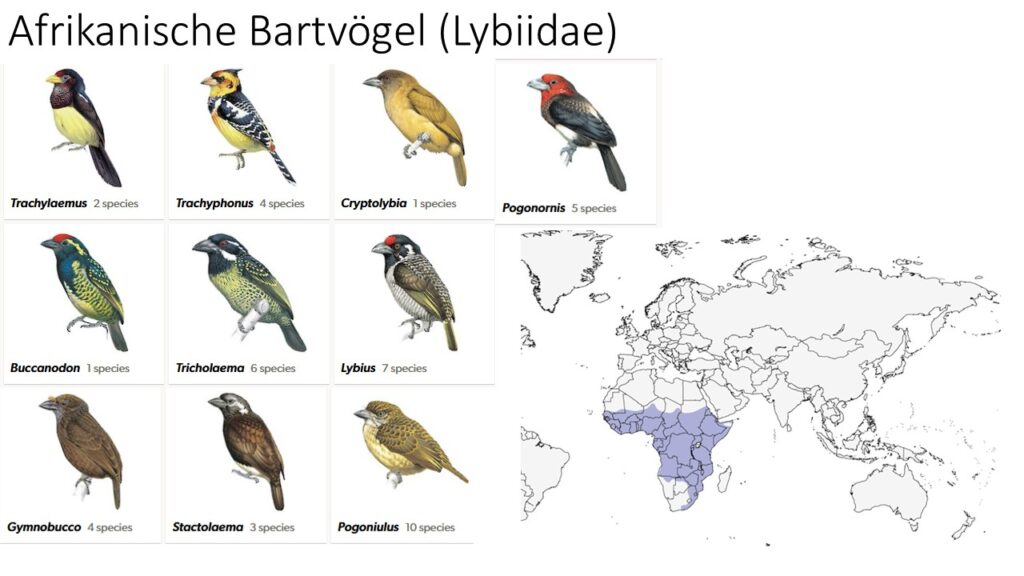
Die Afrikanischen Bartvögel (Lybiidae) sind mit bis zu 51 Arten in 9-10 Gattungen die artenreichste Bartvogelfamilie. In Afrika bewohnen Bartvögel nicht nur die tropischen Regenwälder, viele Arten kommen auch in der Savanne vor. Hier finden sich innerhalb der Gattung der Zwergbartvögel (Pogoniulus), bei denen viele Arten etwa 10 cm lang werden, die kleinsten Bartvögel der Welt. Ein besonders auffälliger Bartvogel der afrikanischen Savannen ist der Flammenkopf-Bartvogel (Trachyphonus erythrocephalus), dessen Lautäußerungen zu den typischen Lauten der ostafrikanischen Savanne gehören. Typische Vertreter der afrikanischen Wälder sind z. B. der Gelbfleck-Bartvogel (Buccanodon duchaillui) und die Gattung der Borstenbärtlinge (Gymnobucco), bei denen die meisten Arten ein unbefiedertes Gesicht haben. Afrikanische Bartvögel ernähren sich wie ihre Verwandten in Asien und Südamerika hauptsächlich von Insekten und Früchten (Winkler et al. 2015, 2020e, Del Hoyo et al. 2002, Del Hoyo 2020).
Bartvögel und Tukane sind fossil schlecht überliefert. Fossile Bartvögel sind aus dem Miozän von Floria bekannt und werden in die Gattung Capitonides gestellt. Weiterhin sind einige Funde aus dem Miozän Europas bekannt. 2019 wurde ein Fossil in Sibirien entdeckt, welches als Stammgruppenvertreter der Bartvögel angesehen wird und vorerst ebenfalls in die Gattung Capitonides gestellt wird. Ein weiteres fossiles Taxon ist Rupelramphastoides aus dem Oligozän in Deutschland. Er ähnelt oberflächlich den Tukanen, weist aber eine Reihe urtümlicher Merkmale auf, sodass seine eindeutige taxonomische Stellung unsicher ist (Mayr 2005, 2009, 2016, Ball 1969, Volkova 2020).
Honiganzeiger (Indicatoridae)
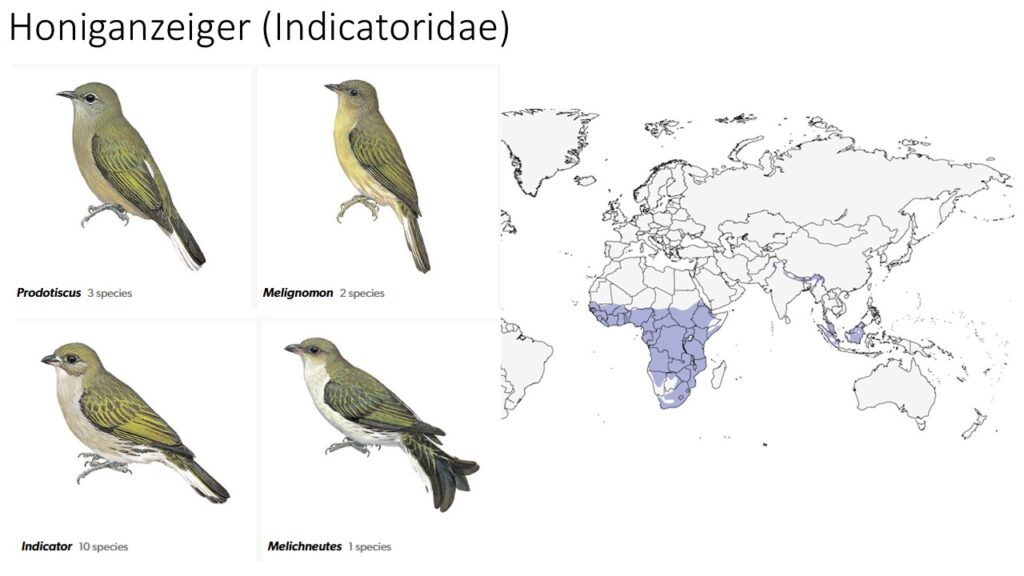
Von den 17 Arten in 4 Gattungen der Honiganzeiger kommen 15 Arten in Afrika, überwiegend in den Regenwäldern, vor. Die zwei anderen Arten leben in Indonesien bzw. im Himalaya. Honiganzeiger ernähren sich hauptsächlich von Insekten, zu den charakteristischen Merkmalen der Familie gehört jedoch, dass alle auch Bienenwachs fressen. Honiganzeiger sind in der Lage, Bienenwachs zu verdauen, weil in ihrem Darm darauf spezialisierte Bakterien leben. Honig fressen sie dagegen nicht. Honiganzeiger erreichen ausgewachsen eine Körperlänge zwischen 10 und 20 Zentimeter und wiegen zwischen 10 und 55 Gramm. Der Schnabel ist bei den meisten Arten kurz und kräftig. Das Gefieder ist unauffällig und von bräunlichem, gräulichem oder olivfarbenem Ton (Winkler et al. 2015, 2020f, Del Hoyo et al. 2002, Del Hoyo 2020).
Ihren Namen haben diese Vögel aufgrund einer außergewöhnlichen Verhaltensweise, die bei drei Arten beobachtet wurde: dem Großen, Kleinen und Schuppen-Honiganzeiger (Indicator indicator, I. minor, I. variegatus). Vertreter dieser Arten ziehen allein oder in kleinen Gruppen umher und lenken die Aufmerksamkeit eines Menschen durch lautes Rufen auf sich um diesen an ein Bienennest zu leiten. Wird das Bienenest vom Menschen gefunden und aufgebrochen – wozu der Honiganzeiger nicht in der Lage ist – frisst der Honiganzeiger die verbliebenen Insekten und Wabennester. Während diese Kooperation mit dem Menschen dokumentiert ist, bleibt die Wechselbeziehung mit anderen Tierarten fraglich. Unbekannt ist, ob auch die anderen Arten ein solches Verhalten zeigen. Die Behauptung, dass der Honiganzeiger auch dem Honigdachs bei der Suche nach Honig hilft scheint eher ein populärer Mythos zu sein (u. a. auch verfilmt in der Dokumentation die Lustige Welt der Tiere), der sich wenig auf empirisches Material stützt (van der Wal et al. 2023, 2025, Dean et al. 1990, Spottiswoode et al. 2016, Wood et al. 2014, Hooper 2014, Isack & Reyer 1989, Marlowe et al. 2014).
Von 11 Arten ist zudem bekannt, dass sie Brutparasitismus betreiben, den Kuckucken ähnlich. Ein Weibchen legt jährlich etwa 20 Eier jeweils einzeln in die Nester von Höhlenbrütern. Parasitiert werden unter anderem höhlenbrütende Spechte, Bienenfresser, Baumhopfe, Glanzstare und Eisvögel. Arten der Gattung Prodotiscus parasitieren auch bei einigen Singvogelarten wie Fliegenschnäppern und Brillenvögel, die offene Nester bauen. Häufig pickt das Weibchen zuvor die Eier an oder entfernt ein oder mehrere Eier aus dem Gelege des Wirtsvogels. Die Eier sind weiß, ähnlich wie die der höhlenbrütenden Wirtsvögel. Es wird vermutet, dass dies weniger eine Anpassung an die Wirtsvögel, sondern vielmehr ein Indiz dafür ist, dass die Honiganzeiger ursprünglich ebenfalls Höhlenbrüter waren. Nach dem Schlüpfen tötet der junge Honiganzeiger – zu diesem Zeitpunkt noch nackt und blind – die anderen Nestbewohner mit seinem hakenförmigen Eizahn. Er verlässt nach etwa vier Wochen das Nest.
Spechte (Picidae)
Mit über 30 Gattungen und 235-256 Arten sind Spechte die artenreichste Gruppe innerhalb ihrer Ordnung. Sie sind fast weltweit verbreitet, fehlen aber in baumarmen Lebensräumen wie der Tundra oder Wüste. Außerdem fehlen sie in Australien, Neuguinea, Neuseeland, Madagaskar und den pazifischen Inseln. Die größte Artenvielfalt findet sich in Mittel- und Südamerika, wo über 100 Arten vorkommen. In Mitteleuropa gibt es 10 Arten. Die häufigste Art ist der Buntspecht. Zudem finden sich hierzulande auch Klein-, Mittel-, Blut-, Grün-, Grau-, Schwarz-, Weißrücken und Dreizehenspecht, sowie der Wendehals. Zu den kleinsten Spechtarten gehört der Goldstirn-Zwergspecht (Picumnus aurifrons) aus Südamerika mit einer Körperlänge von 7,5 cm und einem Gewicht von 8 bis 10 g. Der Puderspecht (Mulleripicus pulverulentus) aus Südostasien ist mit 50cm Körperlänge und etwa 500g die größte heute lebende Spechtart. Größer wurde der Kaiserspecht (Campephilus imperialis) aus Mexiko, dieser ist aber wahrscheinlich wie der Elfenbeinspecht (Campephilus principalis) möglicherweise ausgestorben (Winkler et al. 2015, 2020g, Del Hoyo et al. 2002, Del Hoyo 2020).
Die anatomischen Merkmale der Spechte
Die Gefiederfarben vieler Arten basieren auf Oliv und Braun, einige sind gescheckt, andere sind auffällig schwarz, weiß und rot gemustert, und viele haben einen Kamm oder Federbüschel auf dem Scheitel. Mit Ausnahme des asiatischen Reinwardtspechts (Reinwardtipicus validus) unterscheiden sich die Geschlechter kaum.
Sie haben wie alle Spechtvögel die zygodactylen Füße, die sich gut zum Greifen von Baumstämmen eignen. Von dieser Zehenanordnung weichen einige Arten, wie der Dreizehenspecht ab. Hier ist eine hintere Zehe reduziert und wird durch eine andere ersetzt, die optional nach hinten drehen kann. Spechte können senkrecht an Baumstämmen hinaufsteigen. Zusätzlich zu ihren starken Krallen und Füßen haben Spechte kurze, kräftige Beine. Die Schwänze der Spechte, mit Ausnahme der Zwergspechte und Wendehälse, sind versteift und helfen als Stütze beim Baumklettern. Spechte haben kräftige Schnäbel, mit denen sie in Bäume bohren und trommeln, und lange, klebrige Zungen, mit denen sie ihre Nahrung (Insekten und Larven) herausziehen. Der Schnabel besteht aus drei Schichten: einer äußeren Hülle, Rhamphothek genannt, die aus Schuppen aus Keratinproteinen besteht, einer inneren Knochenschicht mit einem großen Hohlraum und mineralisierten Kollagenfasern und einer mittleren Schicht aus porösem Knochen, die die beiden anderen Schichten miteinander verbindet. Um Hirnschäden durch die schnellen und wiederholten kräftigen Stöße zu vermeiden, verfügen Spechte über eine Reihe von physischen Merkmalen, die ihr Gehirn schützen. Hervorzuheben ist, dass das Gehirn wenig Gehirnflüssigkeit umgibt, sodass dieses starr im Schädel sitzt und beim Picken nicht hin- und herbewegt, wodurch eine Gehirnerschütterung vermieden wird. Der Schädel besteht aus starken, aber komprimierbaren, schwammartigen Knochen, die sich vor allem an der Stirn und im hinteren Teil des Schädels befinden. Außerdem ist das Zungenbein sehr lang und windet sich durch einen speziellen Hohlraum um den Schädel, wodurch das Gehirn gepolstert wird. Es spielt die Rolle eines Sicherheitsgürtels. Zusammengenommen trägt diese Anatomie dazu bei, dass der Schnabel mechanische Belastungen abfedern kann. Ihre langen, klebrigen Zungen, die mit Widerhaken versehen sind, helfen diesen Vögeln beim Greifen und Herausziehen von Insekten aus einem tiefen Loch im Baum. Ferner ist der Schädel von starken Muskeln umgeben, die als Stoßdämpfer dienen: Diese Muskeln werden kurz vor dem Aufprall gegen das Holz angespannt und absorbieren so einen Großteil der Energie. Außerdem wird die Klopfbewegung extrem geradlinig ausgeführt. Dadurch bleiben Hals und Kopf zueinander starr, und jede horizontale oder vertikale Drehung des Kopfes wird vermieden, so dass nur geringe Scherkräfte wirken können.
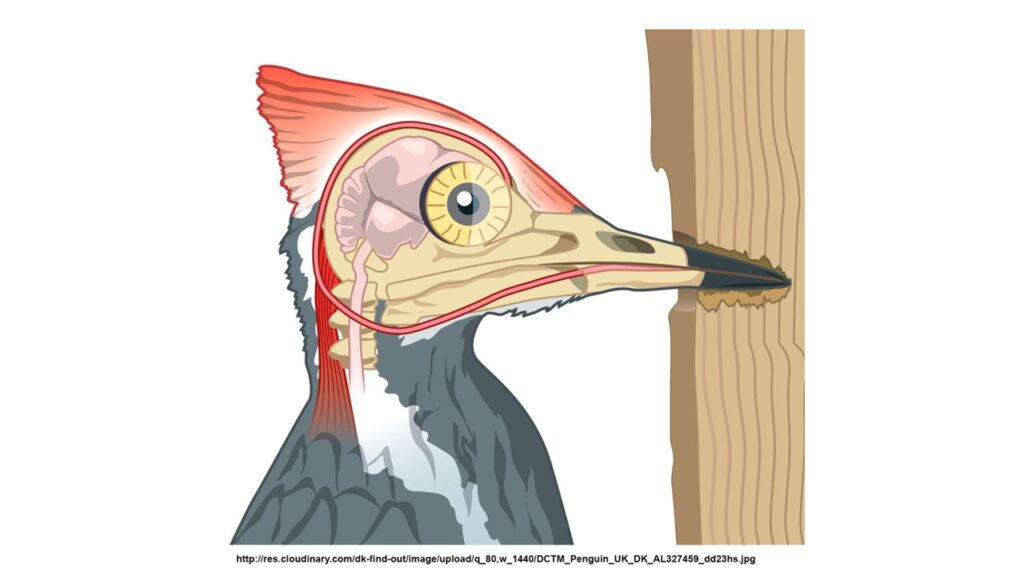
Computersimulationen haben gezeigt, dass 99,7 % der beim Picken erzeugten Energie im gesamten Körper des Vogels verteilt wird, während nur ein kleiner Rest der Energie ins Gehirn geht. Durch das Picken erwärmt sich auch der Schädel des Spechtes, was mit ein Grund dafür ist, dass er oft in kurzen Stößen pickt und dazwischen kurze Pausen einlegt, damit der Kopf abkühlen kann.[14] In der Millisekunde vor dem Kontakt mit dem Holz schließt sich eine verdickte Nickhaut, die das Auge vor umherfliegenden Trümmern schützt.[15] Diese Membranen verhindern auch, dass die Netzhaut reißt. Auch die Nasenlöcher sind geschützt; sie sind oft schlitzförmig und mit speziellen Federn bedeckt.
Ein Specht kann bis zu 20 Schläge pro Sekunde ausführen, jeder Schlag ist vergleichbar mit einem Aufprall des Schnabels mit 25 km/h gegen eine Wand, wobei eine Verzögerung von bis zu 1200 g wirksam werden kann – eine mehrere hundert Mal größere Verzögerung als Astronauten bei einer Landung aus dem All auszuhalten haben (Bock 1999, 2015, Puiu 2017, Wang et al. 2011a,b, Ha et al. 2019 Helmestine 2014, Villard & Cuisin 2004, van Wasserbergh et al. 2022, van Wasserbergh & Mielke 2024, Gibson 2006, May et al. 1976, 1979, Xu et al. 2021).
Lebensweise der Spechte
Die meisten Spechte leben als Einzelgänger, es gibt aber Arten, die in Gruppen leben. Einzelgängerische Arten verteidigen Nahrungsquellen indem sie andere Artgenossen vertreiben. Zu den aggressiven Verhaltensweisen gehören das Stechen mit dem Schnabel, Kopfschütteln, Flügelschlagen, Jagen, Trommeln und Lautäußerungen. Gruppenlebende Arten brüten nicht nur in Gruppen, sondern können sich auch Schwärmen anderer insektenfressender Vogelarten anschließen. Durch den Zusammenschluss mit diesen Schwärmen können Spechte ihre Wachsamkeit gegenüber Raubtieren verringern und ihre Fütterungsrate erhöhen. Spechte sind tagaktiv und halten sich nachts in Höhlen und Spalten auf. Bei vielen Arten wird der Schlafplatz während der Brutzeit zum Nistplatz, aber bei einigen Arten haben sie getrennte Funktionen; der asiatische Kurzschwanzspecht (Hemicircus concretus) legt mehrere flache Löcher zum Schlafen an, die sich deutlich von seinem Nistplatz unterscheiden. Die meisten Vögel übernachten allein und vertreiben Eindringlinge von ihrem gewählten Platz, aber der Magellanspecht (Campephilus magellanicus) hat kooperative Schlafplätze.
Das Trommeln mit ihrem Schnabel ist eine Form der Kommunikation, wobei jede Art ein eigenes Trommel-Muster hat, das sich durch die Anzahl der Schläge, der Dauer des Trommelns und der Pausen dazwischen unterscheidet. Das Trommeln dient der gegenseitigen Erkennung von Artgenossen und spielt eine Rolle bei Balzritualen. Es kann zuverlässig zur Unterscheidung mehrerer Arten in einer Region verwendet werden. Die Kadenz (d. h. die durchschnittliche Anzahl der Trommelschläge pro Sekunde) ist innerhalb der Arten stark konserviert und es scheint auch „Diakelte“ zwischen einzelnen Populationen nicht zu geben, wie man es beim Gesang der Singvögel kennt. Das Trommeln bei Spechten wird durch eine Reihe von Kernen im Vorderhirn gesteuert, die den Hirnregionen ähneln, die dem Erlernen und der Produktion von Gesang bei vielen Singvögeln zugrunde liegen. Spechte verfügen nicht über eine so breite Palette von Gesängen wie Singvögel, und ihre Laute sind in der Regel einfacher strukturiert. Diese Rufe werden bei der Balz, bei Revierstreitigkeiten oder bei Alarmrufen verwendet. Jede Art hat ihr eigenes Rufspektrum und Nestlinge geben oft laute Bettelrufe aus ihrer Nisthöhle von sich. Die Wendehälse haben hingegen einen musikalischeren Gesang (Miles et al. 2018, 2020, Schuppe et al. 2021, 2022, Dodenhoff et al. 2001, Cárdenas-Posada et al. 2023).
Die meisten Spechtarten ernähren sich überwiegend von Insekten, aber insgesamt zeichnet sich die Familie durch ihre Flexibilität bei der Ernährung aus, wobei viele Arten auch Opportunisten sind. Auf dem Speiseplan stehen Ameisen, Termiten, Käfer und ihre Larven, Raupen, Spinnen, andere Gliederfüßer, Vogeleier, Nestlinge, kleine Nagetiere, Eidechsen, Früchte, Nüsse und Säfte. Spechte können Geräusche aus dem Inneren des Holzes hören, die ihm anzeigen, wo das Anlegen eines Lochs ergiebig wäre.
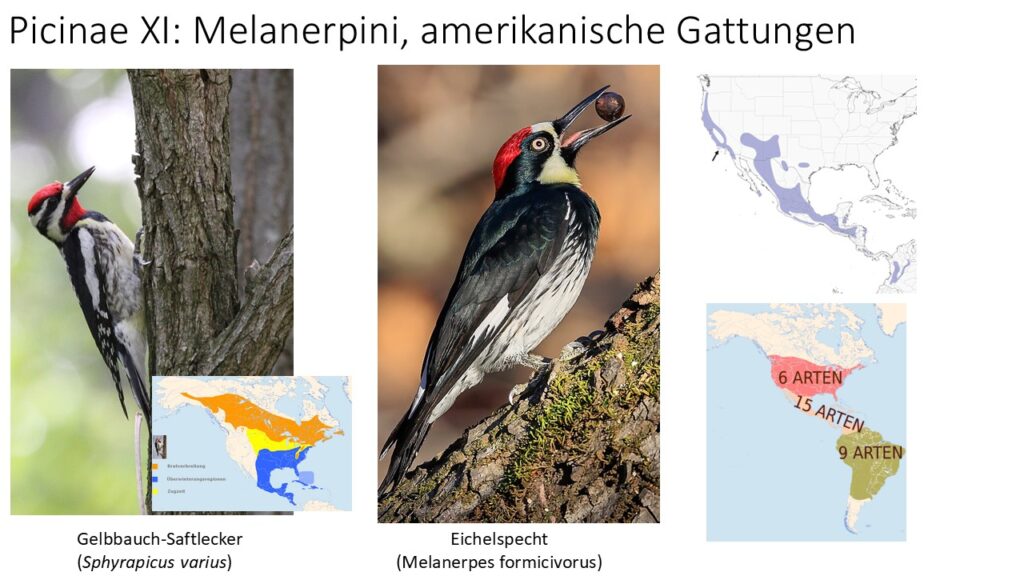
Einige Arten, wie z. B. der nordamerikanische Rotnacken-Saftlecker (Sphyrapicus nuchalis) fangen Insekten auch im Flug und viele Arten stochern in Ritzen und unter Rinde oder sammeln Beute von Blättern und Zweigen. Der asiatische Rötelspecht (Micropternus brachyurus) hat sich auf Baumameisen spezialisiert und der afrikanische Termitenspecht (Pardipicus nivosus) ernährt sich von Termiten und nistet in deren Bauten.
Aus ökologischer Sicht tragen Spechte zur Gesunderhaltung der Bäume bei, indem sie sie vor Massenbefall bewahren. Durch ihre besonderen Fähigkeiten können Spechte den Baumsaft gewinnen, der für einige Arten eine wichtige Nahrungsquelle darstellt. Am bekanntesten hierfür ist die Gattung der Saftlecker (Sphyrapicus) aus Nordamerika.
Alle Mitglieder der Familie sind Höhlenbrüter und bevorzugen Baumhöhlen. Einige Arten, wie Wüstengoldspecht (Colaptes chrysoides), brüten auch in Kakteen und der Bambusspecht (Gecinulus viridis) spezialisiert sich auf Bambus. Ein typisches Nest hat ein rundes Eingangsloch, in das der Vogel gerade hineinpasst, und führt zu einer vergrößerten vertikalen Kammer darunter. Es wird kein Nistmaterial verwendet, abgesehen von einigen Holzspänen, die bei der Ausgrabung anfallen; andere Holzspäne werden großzügig auf den Boden gestreut, um den Standort des Nests sichtbar zu machen. Es dauert etwa einen Monat, bis die Arbeit abgeschlossen ist, und die verlassenen Löcher werden von anderen Vögeln und Säugetieren genutzt, die Höhlenbrüter sind und nicht in der Lage, ihre eigenen Löcher zu graben. Spechte sind in der Regel monogam, wobei einige Arten kooperativ brüten und bei einigen anderen von Polygamie berichtet wird. Polyandrie, bei der ein Weibchen zwei Bruten mit zwei verschiedenen Männchen aufzieht, wurde beim Bahamaspecht (Melanerpes superciliaris) beobachtet. Ein weiteres ungewöhnliches Sozialsystem ist das des Eichelspechts (Melanerpes formicivorus), bei dem Gruppen von bis zu 12 Individuen brüten und bei der Aufzucht der Jungen helfen. Ein Paar arbeitet zusammen, um das Nest zu bauen, die Eier auszubrüten und die Jungtiere aufzuziehen. Bei den meisten Arten übernimmt jedoch das Männchen den größten Teil des Nestbaus und die Nachtschicht beim Ausbrüten der Eier (Kotaka & Matsuoka 2002, Short 1979, Wiktander et al. 2000, Willimont et al. 1991).
Diversität der Spechte
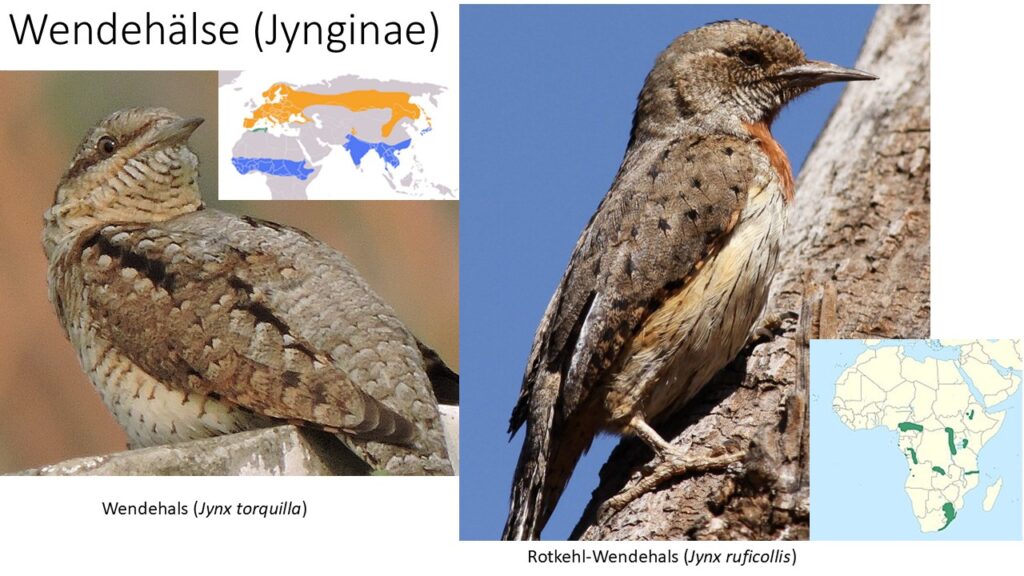
Spechte werden in vier Unterfamilien aufgeteilt (Sangster et al. 2022, Shakya et al. 2017, Fuchs et al. 2006, 2008, Fuchs & Pons 2015. Benz et al. 2006, Winkler et al. 2015, 2020g, Del Hoyo et al. 2002, Del Hoyo 2020). Die Unterfamilie Wendehälse (Jynginae) hat eine Gattung mit zwei Arten, die in Europa, Afrika und Asien leben. Ihren Namen haben diese Vögel von ihrer Fähigkeit, ihren Kopf um fast 180° zu drehen.
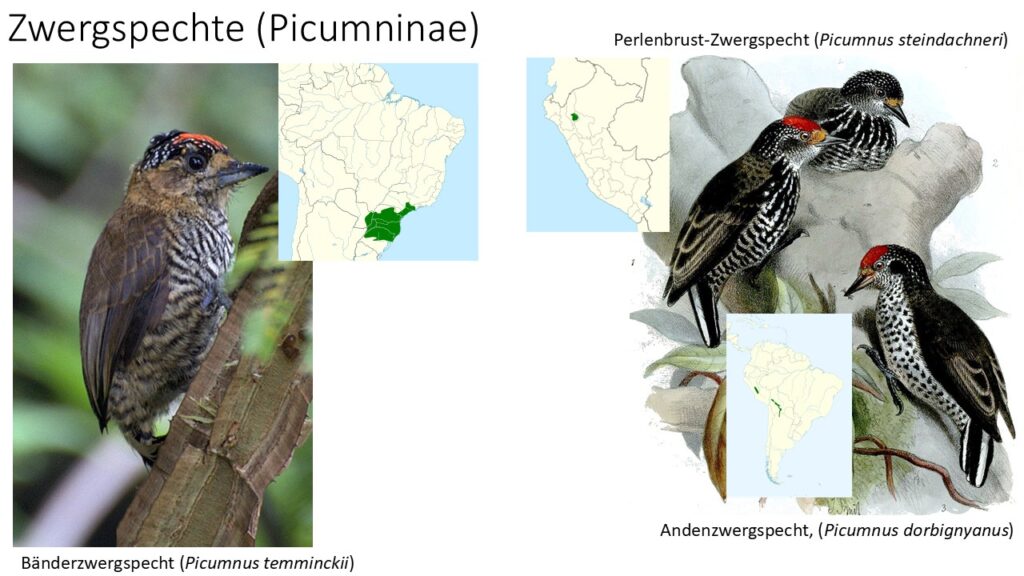
Die zweite Unterfamilie sind die Zwergspechte (Picumninae) mit einer Gattung (Picumnus) und 25 bis 27 Arten. Im Gegensatz zu den Echten Spechten haben die Zwergspechte keinen Stützschwanz, da ihre Schwanzfedern nicht steif genug sind. Da ihr Schnabel nicht so stabil ist, bauen sie ihre Bruthöhlen nicht selbst, sondern nutzen verlassene Spechthöhlen. Sie sind durch einen relativ großen Kopf und eine lange Zunge gekennzeichnet und gehören zu den kleinsten Spechten. Eine Art lebt in China und Südostasien, die anderen in Süd- und Mittelamerika.
Die Unterfamilie der Mausspechte (Sasiinae) umfasst zwei Gattungen mit drei Arten, von denen eine Gattung (Sasia) mit zwei Arten in Südostasien und die dritte Art in Afrika lebt und in eine eigene Gattung (Verreauxia africana) gestellt wird. Diese kleinen Spechte wurden früher ebenfalls zu den Zwergspechten gezählt, gelten aber nach neusten Untersuchungen zu einer eigenen Unterfamilie.

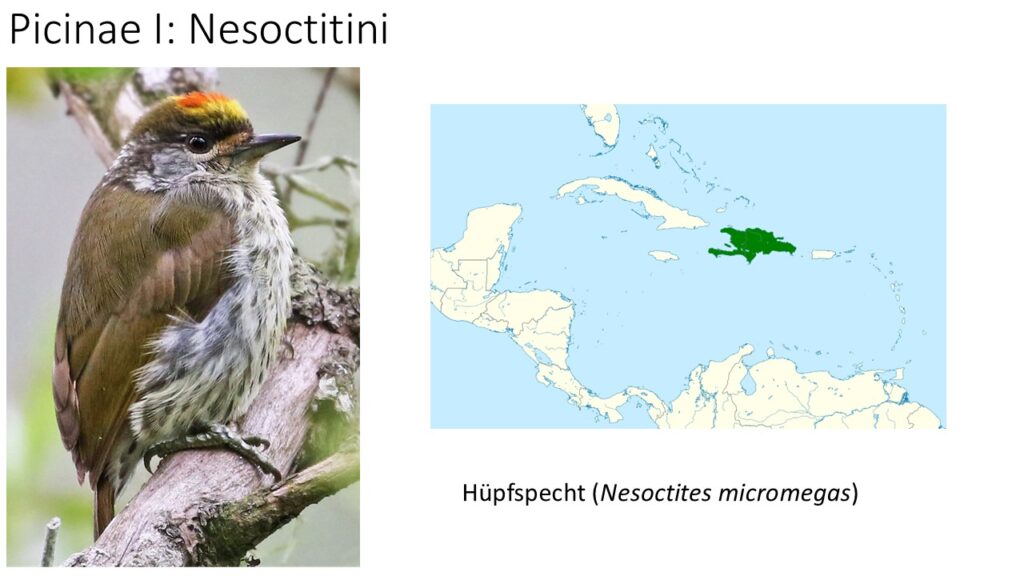
Die mit Abstand größte Unterfamilie stellen die Echten Spechte (Picinae) dar. Die etwa 30 Gattungen mit über 200 Arten werden in fünf Gattungsgruppen zusammengefasst. Zwei Gattungsgruppen sind in ihrer Vielfalt überschaubar. Die Nesoctitini haben nur eine Gattung mit einer Art, dem Hüpfspecht (Nesoctites micromegas), der in der Karibik vorkommt und die Gruppe der Hemicircini haben eine Gattung (Hemicircus) mit zwei Arten in Südostasien.

14 Gattungen zählen zur Gattungsgruppe der Picini. Hierzu gehört auch die Gattung Picus mit 13-15 Arten, die in Europa und Asien vorkommen, mit einem Verbreitungsschwerpunkt in den Tropen Asiens. In Mitteleuropa leben Grünspecht (Picus viridis) und Grauspecht (Picus canus). Weitere rein asiatische Gattungen sind der Rötelspecht (Micropternus brachyurus) mit einer Art, Meiglyptes mit 3-4, die Bambusspechte (Gecinulus) mit 2-3, Dinopium mit 5-6, Chrysophlegma mit 3-4 und Mulleripicus mit 4 Arten. In Afrika kommen die Gattungen Pardipicus mit 2 Arten, der Erdspecht (Geocolaptes olivaceus) mit einer Art und die Fleckenspechte (Campethera) mit 10-13 Arten vor. Die Gattung Dryocopus hat 6-7 Arten, die in Europa, Asien, Nord- und Südamerika vorkommen. Hierzu zählt auch der in Mitteleuropa vorkommende Schwarzspecht (Dryocopus martius). Die Gattung Celeus hat 12-15 Arten in Mittel- und Südamerika. Ebenfalls auf Mittel- und Südamerika beschränkt ist die Gattung Piculus mit 7 Arten. Die Gold- oder Krummschnabelspechte (Colaptes) kommen mit 13-19 Arten in Nord- und Südamerika vor.






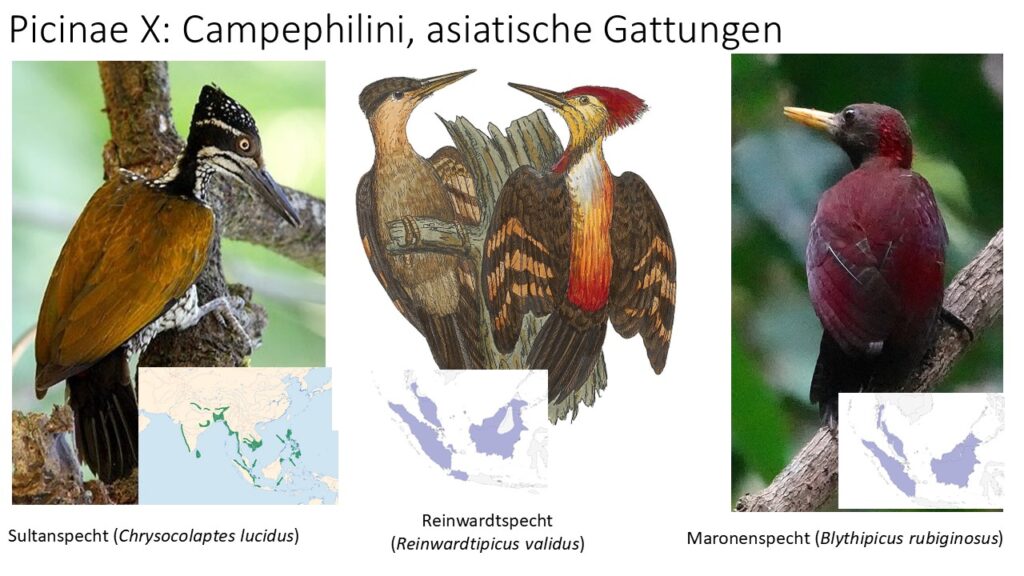
Die Gattungsgruppe der Campephilini hat vier Gattungen. Die Langhaubenspechte (Campephilus) haben 11 bis 12 Arten in Nord- und Südamerika, von denen zwei – der Elfenbeinspecht (Campephilus principalis) und der Kaiserspecht (Campephilus imperialis) – möglicherweise ausgestorben sind. Die Gattung Chrysocolaptes hat 8-10 Arten in Südostasien. Ebenfalls auf Südostasien beschränkt ist die Gattung Reinwardtipicus mit einer Art – dem Reinwardtspecht (Reinwardtipicus validus). Die Gattung Blythipicus hat zwei Arten, die ebenfalls in Südostasien vorkommen.

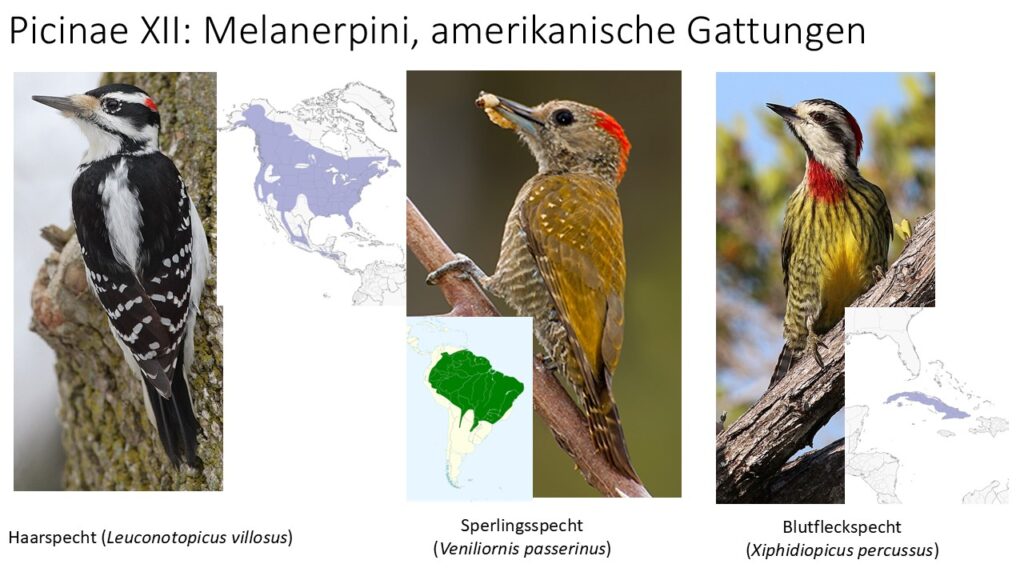
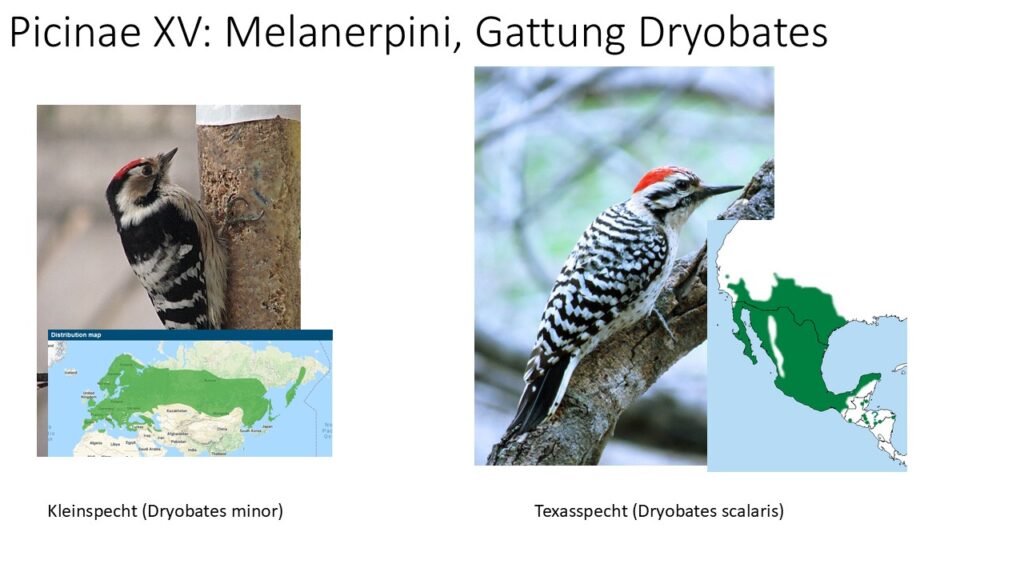
Die Gattungsgruppe Melanerpini hat 13 Gattungen. Die Saftlecker (Sphyrapicus) umfassen vier Arten aus Nordamerika. Ausschließlich in Nord- und Südamerika heimisch sind die Gattungen Melanerpes mit 23-24 Arten und Leuconotopicus mit 6 Arten. In Mittel- und Südamerika kommt die Gattung Veniliornis mit 14 Arten vor. Die Gattung Xiphidiopicus hat nur eine Art, den Blutfleckspecht (Xiphidiopicus percussus), der in Kuba lebt. In Asien kommen die Gattungen Yungipicus mit 7 Arten vorwiegend in den Tropen und Leiopicus mit einer Art auf dem indischen Subkontinent vor. In Afrika leben die Gattungen Chloropicus mit 3 Arten und Dendropicos mit 12-13 Arten. Zur Gattung Dendrocoptes gehören drei Arten, die in Europa und Asien vorkommen. Hierzu zählt auch der in Mitteleuropa heimische Mittelspecht (Dendrocoptes medius). In diese Gattung gehört auch der Arabienspecht (Dendrocoptes dorae), der früher in die afrikanische Gattung Dendropicos gestellt wurde. Die Gattung Dryobates hat 5-6 Arten und kommt in Europa, Asien und Nordamerika vor, darunter der auch der in Mitteleuropa brütende Kleinspecht (Dryobates minor). Die Gattung Picoides lebt in den gemäßigten Zonen Nordamerikas und Eurasiens, darunter der Dreizehenspecht (Picoides tridactylus). Die Gattung Dendrocopos hat 12-13 Arten, die über weite Teile des tropischen und gemäßigten Asiens, sowie Europa vorkommen. In diese Gattung gehören auch Weißrücken- (Dendrocopos leucotis), Blut- (Dendrocopos syriacus) und Buntspecht (Dendrocopos major), die in Mitteleuropa vorkommen.





Evolution der Spechte
Die frühesten Spechtfossilien stammen aus dem Oligozän Europas und Nordamerikas vor 25 Mio. Jahren, die der Unterfamilie der Zwergspechte ähneln. Hier seien fossile Gattungen wie Paleopicus und Piculoides zu erwähnen. Wahrscheinlich entstand aber diese Unterfamilie schon im Eozän. Die modernen Unterfamilien scheinen im Vergleich dazu recht jung zu sein; bis zum mittleren Miozän vor 10-15 Mio. Jahren scheinen alle Spechte kleine oder mittelgroße Vögel gewesen zu sein, die einer Mischung aus Zwergspechte und Wendehals ähneln. Eine in fossilem Bernstein eingeschlossene Feder aus der Dominikanischen Republik, die auf etwa 25 Mya datiert wird, scheint jedoch darauf hinzuweisen, dass die echten Spechte zu diesem Zeitpunkt bereits eine eigenständige Linie waren. Der früheste afrikanische Fund der echten Spechte stammt aus dem Pliozän Südafrikas und gehört zur Gattung Australopicus. Aus dem Miozän Nordamerikas sind die Gattungen Palaeonerpes und Pliopicus bekannt. Des Weiteren finden sich noch eine Reihe von Stammgruppenvertretern, deren taxonomische Einordnung unsicher ist. Hierzu gehören die Gattungen Rupelramphastoides aus dem Oligozän von Deutschland, Picavus aus dem Oligozän Tschechiens und Miopico aus dem Miozän Marokkos (Mayr 2009, 2016, Mayr & Gregorová 2012, Manegold & Louchart 2012, Grimaldi & Case 1995).
Der letzte gemeinsame Vorfahre der Spechte lebte vor etwa 45 Mio. Jahren in Eurasien und trennte sich von seiner Schwestergruppe, den Honiganzeigern. Er glich eher den Zwergspechten und hatte noch nicht die spezialisierten Anpassungen der eigentlichen Spechte, die sich später im Verlauf der Evolution entwickelten.
Die Spechtzunge – ein Problem für die Evolutionstheorie?[1]
Spechte haben eine Reihe außergewöhnlicher Merkmale und daher haben einige Kreationisten die Behauptung aufgestellt, dass ihre Merkmalskombination zu komplex sei, als dass sie evolutionär entstanden sein könnte, wobei sie sich auf die lange und komplex gebaute Zunge der Spechte konzentrieren.
Die Spechtzunge ist außergewöhnlich spezialisiert. Im Gegensatz zur menschlichen Zunge, die hauptsächlich aus Muskeln besteht, wird die Zunge der Vögel vom Zungenbeinapparat starr gehalten. Alle Wirbeltiere haben Zungenbeine in der einen oder anderen Form; auch wir haben ein u-förmiges Zungenbein und dieser dient als Ansatzpunkt für bestimmte Muskeln des Rachens und der Zunge.
Das Y-förmige Zungenbein der Vögel reicht jedoch bis zur Zungenspitze. Die Gabelung des „Y“ befindet sich direkt vor dem Hals, und in diesem Bereich setzen die meisten Muskeln des Zungenbeins an. Zwei lange Strukturen, die „Hörner“ des Zungenbeins, wachsen von diesem Bereich aus nach hinten und dienen als Ansatzpunkte für die Zungenmuskeln, die am Unterkiefer entspringen. Die Hörner des Zungenbeins können bei einigen Spechtarten bis zum Scheitel des Kopfes wachsen und bei einigen Arten um die Augenhöhle herum oder sogar bis in die Nasenhöhle reichen.
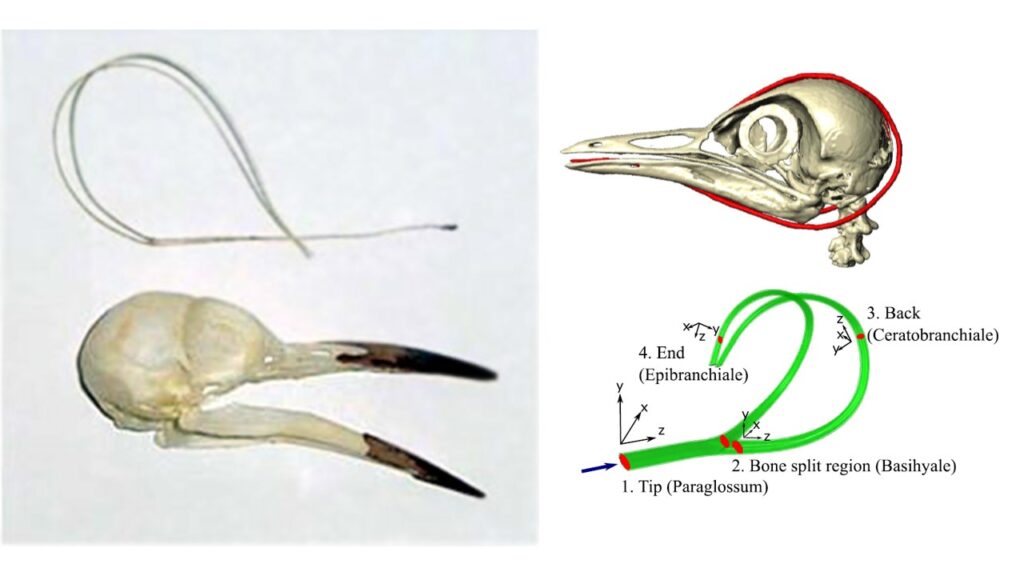
Das ungewöhnliche Aussehen des „Zungenskeletts“ des Spechts hat Kreationisten dazu inspiriert, es als Beispiel für eine Struktur zu verwenden, die zu bizarr ist, um durch zufällige Mutationen entstanden zu sein, die funktionelle Zwischenstufen hervorgebracht haben. Doch das ist natürlich Unsinn, denn die prinzipiell gleiche Konstruktion: Zungenbein und die dazugehörigen Muskeln, Sehen und Bänder, die das Zungenbein mit dem Unterkiefer, Kehlkopf und Schädelbasis verbinden, kommen bei allen Vögeln vor. Bei einigen Vogelarten können die Zungenbeinhörner nach vorne und von oben in die Nasenhöhle hineinwachsen.
Die Zungenbeinhörner dienen als Stützstruktur und kommen bei verschiedenen Vogelarten in unterschiedlicher Länge vor. So hat das Zungenbein der Hühner, die nicht näher mit den Spechten verwandt sind, alle wesentlichen Merkmale der Spechte. Bei Hühnern erstrecken sich die Zungenbeinhörner auf beiden Seiten des Halses nach hinten und rollen sich dann hinter den Ohren zum Hinterkopf auf. Umgeben sind die Zungenbeine von einer Hülle mit Gleitflüssigkeit, auf der sie auf und ab gleiten, wenn die Zunge hinein- oder herausgezogen wird.
Diese Zungenbeinhörner dienen als Ansätze für Muskeln (Musculi branchiomandibularis), die durch die Hülle nach unten verlaufen und in der Mitte des Unterkiefers ihren Ursprung haben. Die Kontraktion dieser Muskeln zieht die Hörner und den gesamten Zungenbeinapparat nach vorne und gegen den Schädel und stößt die Zunge wie einen Speer aus dem Mund. Vergleicht man also das Zungenbein von Hühnern mit jenen der Spechte lassen sie sich klar homologisieren – sie sind bei Spechten halt nur viel länger. Im Grunde genommen kommt es bei Spechten nur zu einer Verlängerung der Zungenbeinhörner und der dazugehörigen Muskeln – etwas, was man bei der Entwicklung von Spechtküken selbst beobachten kann.
Bei neugeschlüpften Spechten reichen seine Zungenhörner nur bis hinter die Ohren, wie bei einem Huhn. Mit zunehmendem Alter werden sie, inklusive der Muskeln länger und wölben sich nach vorne über den Kopf in die Nasenhöhle. Erst mit zunehmendem Alter wachsen die Zungenhörner des Spechtes bis zur Oberseite des Kopfes und in die Nasenhöhle. Dies ist aus Anpassungsgründen sinnvoll, da der junge Specht von seinen Eltern gefüttert wird und eine lange Zunge nur hinderlich wäre.
Die genetischen Veränderungen, die für eine solche Modifikation notwendig sind, sind recht gering. Es sind keine neuen Strukturen erforderlich, sondern lediglich eine längere Wachstumsphase, um eine bestehende Struktur zu verlängern. Es ist wahrscheinlich, dass die Spechte mit Mutationen für ein stärkeres Wachstum des Zungenbeinhorns bei den ursprünglichen Spechtarten, die tiefer in den Bäumen nach Futter suchten, einen Fitnessvorteil hatten, da sie ihre Zunge weiter ausstrecken konnten, um ihre Beute zu erreichen. Auch innerhalb der Spechte gibt es eine Variation in der Länge der Zungenbeinhörner. Saftlecker (Sphyrapicus) bohren beispielsweise nur kleine Löcher in Bäume und haben kürzere Zungen als andere Spechtarten, da sie sich hauptsächlich von den Baumsäften (und den Insekten, die daran kleben) ernähren. Ihr Zungenbeinhorn reicht nur bis zum Kleinhirn. Beim Dunenspecht (Dryobates pubescens) reicht das Zungenbein knapp bis zur Mitte der Augenhöhle, beim Elfenbeinspecht (Campephilus principalis) zum vorderen Ende der Augenhöhle, beim Helmspecht (Dryocopus pileatus) bis zum Ansatz des Nasenbeins, beim Rotkopfspecht (Melanerpes erythrocephalus) bis zur Schnabelbasis und beim Goldspecht (Colaptes auratus) bis zur Nasenhöhle.
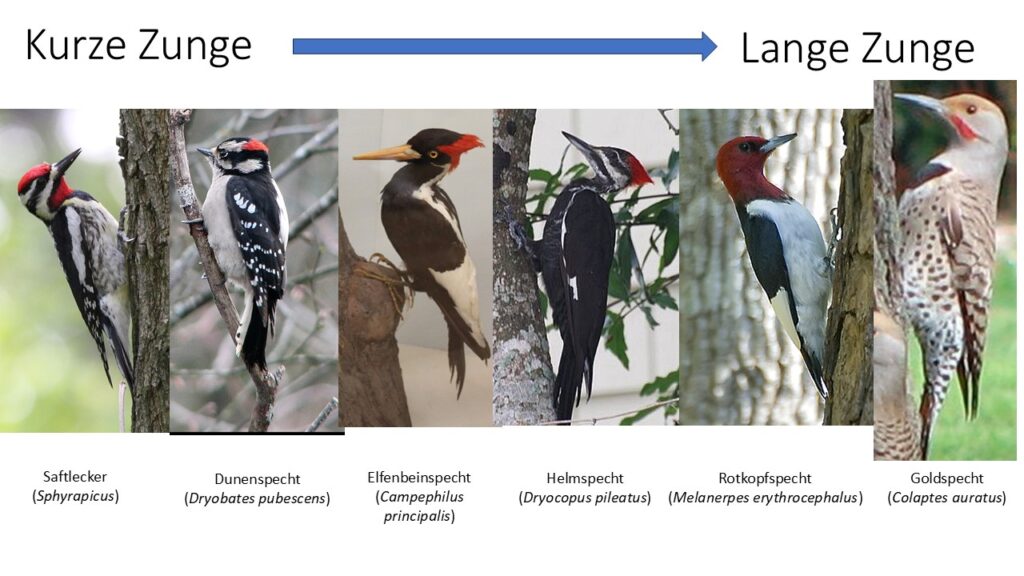
Es gibt also bei den heute lebenden Spechten eine graduelle Verlängerung der Zungenbeinhörner und solch ein Formenkontinuum finden wir auch bei anderen Spechtmerkmalen. Wendehälse und Zwergspechte habe zwar lange Zungen, ihnen fehlt aber die Spezialisierung Löcher in Baumstämme zu meißeln oder die versteiften Schwanzfedern um vertikal die Bäume hochzulaufen. Der Wüstengoldspecht (Colaptes chrysoides) benutzt seine lange Zunge, um Beute vom Boden aufzusammeln. Er hat nur wenige stoßdämpfende Anpassungen und zieht es vor, sich vom Boden zu ernähren oder an verrottendem Holz und Rinde zu knabbern – Gewohnheiten, die auch bei Vögeln außerhalb der Spechtfamilie zu beobachten sind. Spechte sind also eine sehr außergewöhnliche Familie, sie sind aber keine Herausforderung für die Evolutionstheorie (Ryan 2003, Manegold & Töpfer 2013).
Die Afroavaes haben eine Reihe interessante Vogelfamilien: Greifvögel, Eulen, Nashornvögel, Eisvögel Tukane und Spechte. In der nächsten Episode lernen wir die zweite Hauptklade der Telluraves kennen, die Australaves und wie bei den Afroaves beginnen wir hier mit einer Gruppe fleischfressender Vögel.
Literatur
Ballman, P. (1969). A New Species of Fossil Barbet (Aves: Piciformes) from the Middle Miocene of the Nördlinger Ries (Southern Germany). Journal of Vertebrate Paleontology 3 (1): 43-48.
Benz BW, Robbins MB, Peterson AT (2006). Evolutionary history of woodpeckers and allies (Aves: Picidae): placing key taxa on the phylogenetic tree. Molecular Phylogenetics and Evolution. 40 (2): 389–99.
Bock, WJ (1999). Functional and Evolutionary Morphology of Woodpeckers. The Ostrich, 70: 23-31
Bock, WJ (2015). Evolutionary morphology of the woodpeckers (Picidae) – Denisia – 0036: 37 – 54.
Brodkorb, P (1970). An Eocene Puffbird from Wyoming. Rocky Mountain Geology. 9 (1): 13–15.
Cárdenas-Posada, G; Iwaniuk, AN; Fuxjager, MJ (2023). Extractive foraging behaviour in woodpeckers evolves in species that retain a large ancestral brain. Animal Behaviour. 198: 141–152.
David, N (2008). Megalaiminae: the correct subfamily-group name for the Asian barbets. Bulletin of the British Ornithologists‘ Club. 128 (1): 72.
Dean, WRJ. et al. (1990). The Fallacy, Fact, and Fate of Guiding Behavior in the Greater Honeyguide. Conservation Biology. 4 (1): 99–101.
Del Hoyo, J. (2020): All the Birds of the World. Lynx Nature Books
Del Hoyo, J.; Elliot, A.; Sargatal, J., eds. (2002): Handbook of the Birds of the World, volume 7, Jacamars to Woodpeckers, Lynx Edicions, Barcelona.
den Tex, R-J; Leonard, JA (2013). A molecular phylogeny of Asian barbets: Speciation and extinction in the tropics. Molecular Phylogenetics and Evolution. 68 (1): 1–13.
Dodenhoff, DJ, Stark, RD, Johnson, EV c(2001). Do Woodpecker Drums Encode Information for Species Recognition?. The Condor. 103 (1): 143–150.
Duhamel, A et al. (2020). An early Oligocene stem Galbulae (jacamars and puffbirds) from southern France, and the position of the Paleogene family Sylphornithidae. The Auk 137(3): ukaa023, https://doi.org/10.1093/auk/ukaa023
Fuchs, J; Pons, JM (2015). A new classification of the pied woodpeckers assemblage (Dendropicini, Picidae) based on a comprehensive multi-locus phylogeny. Molecular Phylogenetics and Evolution. 88: 28–37.
Fuchs, J. et al. (2006). Molecular phylogeny and biogeographic history of the piculets (Piciformes: Picumninae). In: Journal of Avian Biology. 37: 487-496
Fuchs, J. et al. (2008). Mitochondrial phylogeographic structure of the white-browed piculet (Sasia ochracea): cryptic genetic differentiation and endemism in Indochina. Journal of Biogeography. 35: 565–575.
Gibson L (2006). Woodpecker pecking: how woodpeckers avoid brain injury. Journal of Zoology. 270 (3): 462–465.
Grimaldi DA, Case GR (1995). A feather in amber from the Upper Cretaceous of New Jersey. American Museum Novitates (3126): 1–6.
Ha, N.S., Lu, G. & Xiang, X. (2019). Energy absorption of a bio-inspired honeycomb sandwich panel. J Mater Sci 54, 6286–6300 https://doi.org/10.1007/s10853-018-3163-x
Haffer, J (1969). Speciation in Amazonian Forest Birds. Science 165:131–137
Helmenstine T (2014). Woodpecker Beak Shock Absorbers“ Science Notes. https://doi.org/10.1098/rsif.2014.0274
Hooper, A (2014). Mutualism between man and honeyguide. In: Juliet Clutton-Brock (Hrsg.): The Walking Larder. Patterns of Domestication, Pastoralism, and Predation. Routledge, Kapitel 30
Isack, HA, Reyer, HU (1989). Honeyguides and honey gatherers: interspecific communication in a symbolic relationship. Science 243(4896): 1343–1346
Kotaka N, Matsuoka S (2002). Secondary users of Great Spotted Woodpecker (Dendrocopos major) nest cavities in urban and suburban forests in Sapporo City, northern Japan. Ornithological Science. 1 (2): 117–122.
Ksepka, DT.; Clarke, JA. (2010). Primobucco mcgrewi (Aves: Coracii) from the Eocene Green River Formation: New Anatomical Data from the Earliest Constrained Record of Stem Rollers. Journal of Vertebrate Paleontology. 30 (1): 215–25.
Manegold, A, Louchart, A (2012). Biogeographic and paleoenvironmental implications of a new woodpecker species (Aves, Picidae) from the early Pliocene of South Africa. Journal of Vertebrate Paleontology, 32(4), 926–938. https://doi.org/10.1080/02724634.2012.664597
Manegold A, Töpfer T (2013). The systematic position of Hemicircus and the stepwise evolution of adaptations for drilling, tapping and climbing up in true woodpeckers (Picinae, Picidae). Journal of Zoological Systematics and Evolutionary Research. 51 (1): 72–82.
Marlowe, FW et al. (2014). Honey, Hadza, hunter-gatherers, and human evolution. Journal of Human Evolution 71:119–128
May PR, et al. (1976). Woodpeckers and Head Injury. The Lancet. 307 (7957): 454–455.
May PR, et al. (1979). Woodpecker drilling behavior. An endorsement of the rotational theory of impact brain injury. Archives of Neurology. 36 (6): 370–3. doi:10.1136/bjo.86.8.843. PMC 1771249.
Mayr, G. (2005). A tiny barbet-like bird from the Lower Oligocene of Germany: the smallest species and earliest substantial fossil record of the Pici (Woodpeckers and allies). The Auk 122 (4): 1055–1063.
Mayr, G. (2009). Paleogene Fossil Birds. Heidelberg: Springer
Mayr, G. (2016): Avian Evolution: The Fossil Record of Birds and its Paleobiological Significance. TOPA Topics in Paleobiology.
Mayr, G, Gregorová, R (2012). A tiny stem group representative of Pici (Aves, Piciformes) from the early Oligocene of the Czech Republic. Paläontologische Zeitschrift. 86 (3): 333–343.
Miles MC, Schuppe ER, Ligon RM, Fuxjager MJ (2018). Macroevolutionary patterning of woodpecker drums reveals how sexual selection elaborates signals under constraint. Proceedings of the Royal Society B: Biological Sciences. 285 (1873).
Miles MC, Schuppe ER, Fuxjager MJ (2020). Selection for Rhythm as a Trigger for Recursive Evolution in the Elaborate Display System of Woodpeckers. The American Naturalist. 195 (5): 772–787.
Ostrow, EN et al. (2023). Phylogenomic analysis confirms the relationships among toucans, toucan-barbets, and New World barbets but reveals paraphyly of Selenidera toucanets and evidence for mitonuclear discordance. Ornithology, 140:1–13
Puiu T (2017). Why woodpeckers don’t get headaches. ZME Science.
Ryan, R. (2003). Anatomy and Evolution of the Woodpecker’s Tongue http://www.talkorigins.org/faqs/woodpecker/woodpecker.html
Sangster, G. Gaudin, J., Fuchs, J. (2022). A new subfamily taxon for Sasia and Verreauxia (Picidae). Bulletin of the British Ornithologists’ Club, 142(4):478-479.
Schuppe ER, Rutter AR, Roberts TJ and Fuxjager MJ (2021). Evolutionary and Biomechanical Basis of Drumming Behavior in Woodpeckers. Front. Ecol. Evol. 9:649146.
Schuppe ER, Cantin L, Chakraborty M, Biegler MT, Jarvis ER, Chen CC (2022). Forebrain nuclei linked to woodpecker territorial drum displays mirror those that enable vocal learning in songbirds. PLOS Biology. 20 (9): e3001751.
Shakya, SB et al (2017). Tapping the woodpecker tree for evolutionary insight. Molecular Phylogenetics and Evolution. 116: 182–191.
Short LL (1979). Burdens of the Picid Hole-Excavating Habit. Wilson Bulletin. 91 (1): 16–28.
Spottiswoode, CN et al. (2016). Reciprocal signaling in honeyguide-human mutualism. Science 353 (6297): 387–389.
Tattersall, GJ; Andrade, DV; Abe, AS (2009). Heat Exchange from the Toucan Bill Reveals a Controllable Vascular Thermal Radiator“. Science. 325 (5939): 468–70.
van der Wal, JEM et al. (2023). Do honey badgers and greater honeyguide birds cooperate to access bees‘ nests? Ecological evidence and honey-hunter accounts. Journal of Zoology. 1 (a) – via Zoological Society of London.
van der Wal, JEM et al. (2025). The economic value of human-honeyguide mutualism in Reserva Especial do Niassa, Moçambique. Ecosystem Services, Elsevier, vol. 72(C).
Van Wassenbergh, S; Mielke, M (2024). Why woodpeckers don’t get concussions. Physics Today. 77 (1): 54–55.
Van Wassenbergh, S et al. (2022). Woodpeckers minimize cranial absorption of shocks. Current Anthropology 32(14): 3189–3194.e4
Villard P, Cuisin J (2004). How do woodpeckers extract grubs with their tongues? A study of the Guadeloupe woodpecker (Melanerpes herminieri) in the French Indies. Auk. 121 (2): 509–514.
Volkova, N.V. (2020). The first fossil barbet (Aves, Ramphastidae) from Siberia. J Ornithol 161, 325–332. https://doi.org/10.1007/s10336-019-01719-x
Wang L, Cheung JT-M, Pu F, Li D, Zhang M, Fan Y (2011a). Why Do Woodpeckers Resist Head Impact Injury: A Biomechanical Investigation. PLoS ONE 6(10): e26490. https://doi.org/10.1371/journal.pone.0026490
Wang L, Zhang H, Fan Y (2011b). Comparative study of the mechanical properties, micro-structure, and composition of the cranial and beak bones of the great spotted woodpecker and the lark bird. Science China Life Sciences. 54 (11): 1036–41.
Wiktander U, Olsson O, Nilsson SG (2000). Parental care and social mating system in the Lesser Spotted Woodpecker Dendrocopos minor. Journal of Avian Biology. 31 (4): 447–456.
Willimont LA, Jackson JA, Jackson BJ (1991). Classical polyandry in the West Indian woodpecker on Abaco, Bahamas. Wilson Bulletin. 103: 124–125.
Winkler, DW, Billerman, SM; Lovette, IJ (2015): Bird Families of the World: A Guide to the Spectacular Diversity of Birds. Lynx Edicions, Barcelona.
Winkler, DW, Billerman, SM; Lovette, IJ (2020a). Toucans (Ramphastidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.rampha1.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020b). Toucan-Barbets (Semnornithidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.semnor1.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020c). New World Barbets (Capitonidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.capito2.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020d). Asian Barbets (Megalaimidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.megala2.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020e). African Barbets (Lybiidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.lybiid1.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020f). Honeyguides (Indicatoridae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.indica1.01
Winkler, DW, Billerman, SM; Lovette, IJ (2020g). Woodpeckers (Picidae), version 1.0. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.picida1.01
Winkler, DW, Billerman, SM; Lovette, IJ (2025a). Jacamars (Galbulidae), version 1.1. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.galbul2.01.1
Winkler, DW, Billerman, SM; Lovette, IJ (2025b). Puffbirds (Bucconidae), version 1.1. In Birds of the World (S. M. Billerman, B. K. Keeney, P. G. Rodewald, and T. S. Schulenberg, Editors). Cornell Lab of Ornithology, Ithaca, NY, USA. https://doi.org/10.2173/bow.buccon2.01.1
Witt, C.C. (2004). Rates of Molecular Evolution and their Application to Neotropical Avian Biogeography, Ph.D. dissertation, Louisiana State University
Wood, BM et al. (2014). Mutualism and manipulation in Hadza–honeyguide interactions. Evolution and Human Behavior. 35 (6): 540–546.
Xu P, Ni Y, Lu S, Liu S, Zhou X, Fan Y (2021). The cushioning function of woodpecker’s jaw apparatus during the pecking process. Computer Methods in Biomechanics and Biomedical Engineering. 24 (5): 527–537.
[1] Dieser Abschnitt basiert vor allem auf den Talk Origin Artikel Anatomy and Evolution of the Woodpecker’s Tongue von Rusty Ryan (2003). http://www.talkorigins.org/faqs/woodpecker/woodpecker.html



