Text als pdf
Warum sehen unsere Arme und Beine so komisch aus?[1]
Betrachtet mal eure Gliedmaßen. An einem Ende befinden sich Finger oder Zehen, am anderen Ende Oberarmknochen oder Oberschenkelknochen. Niemand hat Finger in der Mitte seines Arms. Betrachtet auch die subtilen, aber offensichtlichen Unterschiede zwischen unseren Händen und Füßen. Wenn unsere Finger durch Zehen ersetzt würden, würden wir das sicherlich bemerken, denn es sehe echt merkwürdig aus. Trotz dieser Unterschiede ähneln die Knochen unserer Füße den Knochen unserer Hände. Es ist leicht zu erkennen, dass sie ein gemeinsames Muster aufweisen. Und schließlich sollten wir bedenken, dass unsere beiden Hände ebenso wie unsere beiden Füße bemerkenswert ähnlich groß sind. Diese alltäglichen Phänomene werfen für Entwicklungsbiologen faszinierende Fragen auf. Wie kommt es, dass Wirbeltiere vier Gliedmaßen haben und nicht sechs oder acht? Wie kommt es, dass sich der kleine Finger an einem Ende der Gliedmaße und der Daumen am anderen Ende entwickelt? Wie wächst die Vordergliedmaße anders als die Hintergliedmaße? Wie kann die Größe der Gliedmaßen so präzise reguliert werden? Gibt es einen konservierten Satz von Entwicklungsmechanismen, der erklären kann, warum unsere Hände fünf Finger haben, ein Hühnerflügel drei und ein Pferdehuf einen? Die Entstehung der Gliedmaßen ist eines der spannendsten Forschungsfelder innerhalb der Evo-Devo-Forschung. Hiermit schlagen wir auch eine Brücke zur vorherigen Episode, wo wir uns die konstruktionsmorphologischen und paläontologischen Aspekte der Entstehung der Gliedmaßen betrachtet haben.
Werfen wir vorher einen kurzen Blick auf die grundlegende Anatomie der Gliedmaßen um uns an diesen zu orientieren. Eine Tetrapoden-Gliedmaße kann in drei Abschnitte geteilt werden: Der obere Abschnitt ist das Stylopodium und besteht immer aus einem Knochen: Oberarmknochen oder Oberschenkelknochen. Der mittlere Abschnitt ist das Zeugopodium und hat zwei Knochen: Elle und Speiche bzw. Wadenbein und Schienbein. Der untere Abschnitt ist das Autopodium, der aus vielen Knochen besteht und in seiner Anzahl variieren kann: Hier liegen die Handwurzelknochen, Mittelhandknochen und Fingerknochen mit ihren entsprechenden Gegenstücken im Fuß. Finger und Zehen können als Phalangen oder, allgemeiner, als Fingerglieder bezeichnet werden. Die Positionsinformationen, die zum Aufbau einer Gliedmaße benötigt werden, müssen in einem dreidimensionalen Koordinatensystem funktionieren:
- Die erste Dimension ist die proximale-distale Achse, d. h. von der Schulter zum Finger oder von der Hüfte zur Zehe.
- Die zweite Dimension ist die anterior-posteriore Achse, also vom Daumen zum kleinen Finger. Unsere kleinen Finger oder Zehen markieren das hintere Ende, und unsere Daumen oder großen Zehen befinden sich am vorderen Ende.
- Schließlich haben Gliedmaßen eine dorsale-ventrale Achse: Unsere Handflächen (ventral) sind leicht von unseren Fingerknöcheln (dorsal) zu unterscheiden; entsprechendes gilt für unsere Füße.
Grundsätzlich sind die Knochen der Gliedmaßen zunächst knorpelig, aber schließlich wird der größte Teil des Knorpels durch Knochen ersetzt.
Die Gliedmaßenknospe[2]
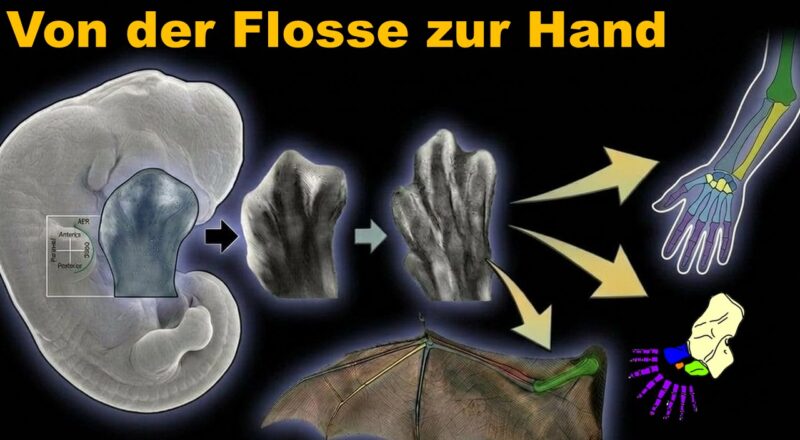
In der Embryonalentwicklung bilden sich die Gliedmaßen aus der sogenannten Gliedmaßenknospe, die aus einem Gliedmaßenfeld hervorgehen. Die Zellen, aus denen sich die Gliedmaßenknospe zusammensetzt, stammen aus dem hinteren lateralen Plattenmesoderm, den angrenzenden Somiten und dem überlagernden Ektoderm der Knospe. Die Zellen des lateralen Plattenmesenchyms wandern innerhalb der Gliedmaßenfelder, um die Vorläuferzellen des Gliedmaßenskeletts zu bilden, während die mesenchymalen Zellen aus den Somiten auf derselben Ebene einwandern, um die Vorläuferzellen der Muskulatur zu bilden. Diese sich ansammelnde heterogene Population von Mesenchymzellen bildet anschließend die Gliedmaßenknospe.
Die Gliedmaßenknospe wird weiter in drei funktionell unterschiedliche Bereiche unterteilt:
- Das Mesenchym, das das Wachstum der Gliedmaßenknospe antreibt, wird als Progressionszonen-Mesenchym (PZ-Mesenchym) oder undifferenzierte Zone bezeichnet.
- Eine Organisatorregion am posterioren Ende der Extremität wird als Zone polarisierender Aktivität (ZPA) genannt. Sie verantwortlich für die antero-posteriore Achsenbildung und beeinflusst maßgeblich Anzahl und Identität von Fingern.
- Eine weitere Organisatorregion ist die Apikale Ektoderm Randleiste (AER), eine Verdickung des Ektoderms an der Spitze der sich entwickelnden Gliedmaßenknospe.
Innerhalb der Gliedmaßenknospe sind verschiedene Gene aktiv, so die Hox-Gene, Sonic Hedgehog, Tbx-Gene, Gene des Wnt-Signalwegs und viele weitere. Wir werden ihre Rolle bei der Gliedmaßenentstehung nach und nach darstellen und uns dann einigen evolutionsbiologischen Fragestellungen widmen.
Da Gliedmaßen im Gegensatz zum Herzen oder Gehirn für das Leben des Embryos nicht lebenswichtig sind, kann man Teile der sich entwickelnden Gliedmaßen experimentell entfernen oder transplantieren oder gliedmaßenspezifische Mutanten erzeugen, ohne die lebenswichtigen Prozesse des Organismus zu beeinträchtigen. Solche Experimente haben gezeigt, dass bestimmte grundlegende „morphogenetische Regeln” für die Bildung einer Gliedmaße bei allen Tetrapoden gleich zu sein scheinen. Transplantierte Teile von Gliedmaßenknospen von Reptilien oder Säugetieren können die Bildung von Hühnergliedmaßen steuern, und aus Froschgliedmaßenknospen entnommene Regionen können die Musterbildung von Salamandergliedmaßen steuern.
Hox-Gene[3]
Die Hox-Gene, die die anerior-posteriore Achse bei Embryonen definieren, bestimmen, an welchen Punkten entlang dieser Achse sich Gliedmaßenknospen bilden. Wirbeltierembryonen entwickeln Segmente, die sogenannten Somiten, deren Schicksal u. a. auch von Hox-Genen beeinflusst wird. An welchen Somiten sich die Gliedmaßenknospen bilden, ist bei den Wirbeltiergruppen unterschiedlich, ist aber in Bezug zu Hox-Gen-Expression entlang der anterior-posterioren Achse konstant. Beispielsweise befinden sich bei Fischen (bei denen die Brust- und Beckenflossen den vorderen bzw. hinteren Gliedmaßen entsprechen), Amphibien, Vögeln und Säugetieren die Vordergliedmaßenknospen an der vordersten Expressionsregion von Hoxc6, der Position des ersten Brustwirbels. Es ist wahrscheinlich, dass die Positionsinformationen aus der Hox-Genexpression dazu führen, dass Mesodermzellen aus den Gliedmaßenbildungsbereichen die Bildung von Gliedmaßenknospen fördert, während anderes Mesodermgewebe die Gliedmaßenbildung aktiv unterdrückt.
Im Vergleich zu Wirbellosen haben Wirbeltiere 4 Hox-Gen-Cluster. In den Gliedmaßenknospen werden Gene des Clusters Hoxa und Hoxd exprimiert, dabei bestimmen die Paraloge von Hox9 und Hox10 das Stylopodium, die Paraloge von Hox11 das Zeugopodium und die Paraloge von Hox12 und Hox13 das Autopodium. Dieses Szenario wurde durch zahlreiche Experimente bestätigt. Als beispielsweise alle drei Hox10-Paraloge (Hox10acd) in Mausembryonen ausgeschaltet wurden, fehlten den Hinterbeinen der resultierenden Mäuse der Oberschenkelknochen und die Kniescheibe, die sich normalerweise im Stylopodium bilden würden. Die Vorderbeine hatten jedoch einen Oberarmknochen, da die Hox9-Paraloge im Stylopodium der Vorderbeine, aber nicht im Stylopodium der Hinterbeine exprimiert werden. Als alle drei Hox11-Paraloge ausgeschaltet wurden, hatten die resultierenden Hinterbeine Oberschenkelknochen, aber weder Schienbeine noch Wadenbeine (und den Vordergliedmaßen fehlten Elle und Speiche). Somit wurden durch das Hox11-Knockout das Zeugopodium beseitigt. In ähnlicher Weise führte der Knockout von Hoxa13 und Hoxd13 zum Verlust des Autopodiums. Menschen, die homozygot für eine HOXD13-Mutation sind, weisen Anomalien an Händen und Füßen auf, bei denen die Finger und Zehen miteinander verwachsen sind, und Menschen mit homozygoten mutierten Allelen von HOXA13 haben ebenfalls Deformationen ihrer Autopodien. Hox-Gene sind entscheidend für die Festlegung des Schicksals entlang jeder Achse der Gliedmaßen, und ihre Expression wird unter durch weitere Signale beeinflusst.
Woher „weiß“ der Embryo wo Arme und Beine entstehen?[4]
Gliedmaßen bilden sich also nicht einfach irgendwo entlang der Körperachse, sondern an bestimmten Stellen. Frühe Studien an Hühnerembryonen haben gezeigt, dass es zwei spezifische Felder des intermediären und Seitenplattenmesoderms gibt, die lange bevor sichtbare Anzeichen von Gliedmaßen auftreten, für ihre Bildung bestimmt sind. Beachtet: das Mesoderm ist eines der Keimblätter, die sich früh im Embryo bilden, aus denen verschiedene Organsysteme hervorgehen. Das Mesoderm selbst kann in verschiedene Regionen eingeteilt werden. Die Rolle des Mesoderms bei der Ausbildung der Gliedmaßenknospen wurde u. a. dadurch verstanden, dass man Zellgruppen entfernte und feststellte, dass die Gliedmaßen sich nicht entwickelten. Wurde diese Zellregionen an andere Stellen transplantiert, bildeten sich dort Gliedmaßen. Wurden diese Zellengruppen z. B. mit Farbstoffen markiert, konnte man sehen, dass sie an der Bildung der Gliedmaßen beteiligt sind.
Bei der Ausbildung der Somiten der Wirbeltiere sind die Signalmoleküle Retinsäure und der Wachstumsfaktor fgf8 beteiligt. Sie bilden ein Konzentrationsgradienten im Embryonalen Gewebe und bestimmen so, z. B. durch gegenseitige Hemmung, die weitere Differenzierung. Fgf8 wird u. a. im Mesoderm des Herzens gebildet, unweit von dem Gliedmaßenfeld, aus dem sich die vorderen Gliedmaßenknospen entwickeln werden. Experimente haben gezeigt, dass eine Expression von Fgf8 die Bildung einer vorderen Gliedmaßenknospe hemmt.
Retinsäure wird in der gesamten Somitenregion des Rumpfes exprimiert und fungiert als Antagonist von Fgf8, indem es dessen Expression unterdruckt. Das Vorhandensein von Retinsäure und die Unterdrückung von Fgf8 in der Nähre des vorderen Gliedmaßenfeldes führt zur Ausbildung der vorderen Gliedmaßenknospe. Experimente, die die Expression der Retinsäure im Vordergliedmaßenfeld unterdrückten führten zu einer Erweiterung der Expression von Fgf8 und einem Ausbleiben der Gliedmaßenknospen.
Interessanterweise scheint bei den hinteren Gliedmaßen die Retinsäure nicht den initiierenden Charakter zu haben. Der Verlust von Retinsäure bei Mäusen hatte keinen Einfluss auf die hinteren Gliedmaßen. Hier dürften andere Gene eine Rolle spielen. Ein Möglicher Kandidat ist das Gen Islet1, welches im hinteren Gliedmaßenfeld vor der Knospenbildung exprimiert wird.
Das Schicksal der vorderen und hinteren Gliedmaßen wird dann durch weitere Gene festgelegt. In den Vordergliedmaßen wird das Gen Tbx5 und in den Hintergliedmaßen Tbx4 exprimiert. Knockout-Experimente zeigen, dass bei Embryonen der Verlust von tbx5 die Ausbildung der Vordergliedmaßen und ein Verlust von tbx4 die Ausbildung von Hintergliedmaßen ausbleibt. Die ursprüngliche Funktion der Tbx-Gene lag wahrscheinlich in der Entwicklung des Herzens und wurden im Lauf der Evolution der Tetrapoden für die Gliedmaßenentwicklung kooptiert. Beim Lanzettfischchen Amphioxus, dem paarige Gliedmaßen fehlen, gibt es nur ein einziges Tbx4/5-Gen, das jedoch bei der Bildung von Gliedmaßen genauso funktionieren kann wie die Gene von Wirbeltieren. Ein eindrucksvoller Beleg dafür ist, dass die Expression des Amphioxus-Tbx4/5-Gens in transgenen Mäusen, bei denen Tbx5 ausgeschaltet worden war, die Entwicklung der Vordergliedmaßen ermöglicht.
In den hinteren Gliedmaßen wird aber noch ein weiteres Gen exprimiert, welches eine Rolle bei der Musterbildung spielt: Pitx1. Wird durch eine Mutation Pitx1 in den Vorderbeinen bei Mäusen exprimiert, ähneln die Muskeln, Knochen und Sehen jenen der Hinterbeine. Mutationen von Pitx1 führen zudem zu verschiedenen Missbildungen der Hintergliedmaßen. Weiterhin werden hinterbeinspezifische Gene durch Pitx1, darunter Hoxc10 und Tbx4, aktiviert.
Nachgeschaltet zur regulatorischen Funktion dieser Transkriptionsfaktoren ist Fgf10, der primäre Induktor für die Bildung von Gliedmaßenknospen, wobei Wnt/β-Catenin und die von ihm initiierten Transkriptionsfaktoren die Fgf10-Signalübertragung aufrechterhalten. Fgf10 hält nicht nur eine die Gliedmaßenbildung fördernde Signalschleife aufrecht, sondern induziert auch direkt die Bildung eines neuen Signalgewebes – der Apikalen Ektoderm Randleiste (AER).
Apikale Ektoderm Randleiste (AER)[5]
Die Apikale Ektoderm Randleiste, kurz AER, beeinflusst die weitere Musterbildung der Gliedmaßenentwicklung. 1948 wurde eine einfache und tiefgreifende Beobachtung gemacht: Wenn das AER aus einer Flügelknospe eines Hühnerembryos im Frühstadium entfernt wird, bildet sich nur ein Oberarmknochen. Wird die AER etwas später entfernt, bilden sich Oberarmknochen, Elle und Speiche. Offensichtlich gibt es in der AER Positionsinformationen, bei der undifferenzierten Mesodermzellen mitgeteilt wurde bestimmte Strukturen auszubilden. Dies geschieht über Konzentrationsgradienten verschiedener Wachstumsfaktoren, wie FGF2, FGF4, FGF8 und FGF9. Der Verlust eines dieser FGFs führt jedoch nur zu leichten bis gar keinen Defekten im Skelettmuster, was darauf hindeutet, dass innerhalb dieser Familie eine erhebliche Redundanz für die Musterbildung der Gliedmaßen besteht. Die genetische Entfernung mehrerer FGF-Gene führte jedoch zu zunehmend schweren und spezifischen Skelettfehlbildungen mit jedem zusätzlich entfernten FGF-Gen.
Fgf10 induziert die Bildung der AER, aktiviert aber auch die Expression von Wnt3A, welches auf das AER wirkt und dafür sorgt, dass diese den Wachstumsfaktor Fgf8 bildet. Während Fgf8, wie bereits angemerkt, vorher die Ausbildung einer Gliedmaßenknospe hemmt, sorgt dessen Bildung in der AER dafür, dass weiterhin Fgf10 produziert wird, um die AER aufrechtzuerhalten. Dasselbe Gen, Fgf8, kann also unter verschiedenen Regulationsbedingungen unterschiedliche Reaktionen hervorrufen. Die weiteren Fgf-Proteine wirken auf die weiteren Mesenchymzellen, einschließlich einer weiteren wichtigen Organisatorzone der Gliedmaßenknospe: der Zone polarisierender Aktivität (ZPA), dessen Genexpression die AER aufrechterhält und vor allem an der Ausbildung des Autopodiums beteiligt ist.
Zone polarisierender Aktivität (ZPA) und Sonic Hedgehog (Shh)[6]
Die Zone der polarisierenden Aktivität (ZPA) ist ein Bereich von Mesenchym-Zellen, also ein lockerer Verband undifferenzierter Zellen, der Signale enthält, die die sich entwickelnde Gliedmaßenknospe anweisen, sich entlang der anterior-posterioren Achse, also vom Daumen zum kleinen Finger, zu bilden. Die Bedeutung der ZPA wurde schon in den 1930er Jahren an Hühnerembryonen erforscht. Wenn Gewebe aus dieser Region aus einer jungen Gliedmaßenknospe entnommen und an eine Stelle auf der anterioren Seite einer anderen Gliedmaßenknospe transplantiert wird, verdoppelt sich die Anzahl der Finger an dem entstehenden Flügel. Darüber hinaus sind die Strukturen des zusätzlichen Satzes von Fingern Spiegelbilder der normalerweise gebildeten Strukturen. Die Polarität bleibt erhalten, aber die Information kommt nun sowohl aus anteriorer als auch aus posteriorer Richtung. Daher wurde dieser Bereich des Mesoderms als Zone der polarisierenden Aktivität (ZPA) bezeichnet. Ähnliche Versuche wurden bei Haien und Rochen durchgeführt und führten zum gleichen Ergebnis: die Flossen wiesen ebenfalls eine Verdoppelung ihrer Fingerstraheln auf. Das entscheidende Signalmolekül der ZPA wurde 1993 entdeckt und ist Sonic Hedgehog (Shh), ein Homolog des Drosophila-Hedgehog-Gens bei Wirbeltieren. Es wird in der Gliedmaßenknospe in der ZPA-Region exprimiert. Wie spezifiziert Sonic Hedgehog die Identität der Finger? Zellen der ZPA, die Sonic Hedgehog exprimieren werden zu den Knochen und Muskeln der Finger. Die Spezifizierung der Finger, also ob z. B. der 5. oder der 4. Finger entsteht, hängt dabei weniger von der Konzentration der Sonic Hedgehog Expression ab, sondern von ihrer Dauer.
Der Unterschied zwischen Finger 4 und 5 besteht also darin, dass die Zellen des weiter hinten liegenden Fingers 5 Sonic Hedgehog länger exprimieren und diesem länger ausgesetzt sind. Finger 3 besteht aus einigen Zellen, die Sonic Hedgehog für einen kürzeren Zeitraum als die von Finger 4 sekretieren, Finger 2 ist nicht von der Dauer, sondern ausschließlich von der Konzentration von Sonic Hedgehog-Expression abhängig und Finger 1 wird unabhängig von Sonic Hedgehog spezifiziert. Tatsächlich bildet sich bei einem natürlich vorkommenden Mutanten-Küken, dem die Sonic Hedgehog-Expression in den Gliedmaßen fehlt, nur Finger 1. Wahrscheinlich wird Finger 1 durch Hoxd13 in Abwesenheit von Hoxd12 spezifiziert.
Sonic Hedgehog aktiviert zudem das Gen Gremlin, das BMP-Gene hemmt und so die Aufrechterhaltung der FGF-Expression und das weitere Wachstum der Gliedmaßenknospen fördert. FGF hemmt wiederum die Repressoren von Sonic Hedgehog, um den positiven Rückkopplungskreislauf zu vervollständigen. Die Stimulation von Sonic Hedgehog lässt die Konzentration von Gremlin weiter ansteigen und BMP-Gene stärker repressieren. Dadurch wächst die Gliedmaßenknospe stärker an. Solange Gremlin in die AER-Region diffundieren kann, werden FGFs weitergebildet und die AER bleibt aufrechterhalten. FGF-Wachstumsfaktoren führen aber zu einem verstärkten Wachstum der Gliedmaßenknospe, was dazu führt, dass sich der Abstand zwischen Gremlin und der AER vergrößert, wodurch nach einem bestimmten Zeitpunkt weniger BMP-Gene unterdrückt und so verstärkt exprimiert werden. Zu diesem Zeitpunkt heben die BMPs die FGF-Synthese auf, die AER und anschließend die ZPA brechen zusammen. Die embryonale Phase der Gliedmaßenentwicklung wird so beendet.
Welche Rolle spielen Hox-Gene bei der Finger-Differenzierung?[7]
Es ist aber keineswegs so, dass nur Sonic hedgehog bei der Entwicklung der Finger eine Rolle spielt. Interessanterweise zeigen Experimente, dass ein völliger knock-out von Sonic hedgehog (und seinem Verstärker Gli3) in der ZPA trotzdem zur Bildung von Fingern führt – es kommt sogar zur Polydactylie, also mehr als 5 Finger. Interessanterweise passt dies auch zum Fossilbericht, da frühe Tetrapoden wie Acantostega mehr als 5 Finger hatten. Wahrscheinlich spielen Hox-Gene bei der Anzahl der Finger ebenfalls eine Rolle.
Während man früher annahm, dass sich die Finger entlang einer Mittelachse bilden, weiß man, dass die Finger in einem Bogen von einer Seite der Hand zur anderen abknospen, also nicht symmetrisch entlang der Mittelachse. Dies passt wunderbar zur Fingerzahl von Acanthostega. Um das moderne Muster von fünf Fingern zu erhalten, muss die Entwicklung nur etwas früher gestoppt werden. Seit dieser Entdeckung wurden die Hox-Gene identifiziert, die diese Entwicklungssequenz steuern, sodass klar ist, dass die Änderung von sieben oder acht Fingern auf nur fünf kein großes Problem darstellt. Es ist lediglich eine kleine Anpassung des Entwicklungszeitpunkts der Knospung der Gliedmaßen erforderlich.
So wird die ZPA auch durch das Vorhandensein von Hoxb8 beeinflusst, das dazu beiträgt, die hintere Grenze der Vordergliedmaßenknospe zu definieren. Wird die ZPA gebildet wirkt sie rückkoppelnd auf das Expressionsmuster der Hoxd-Gene. Dabei aktiviert Sonic Hedgehog eine Gruppe von Enhancern, die als globale Kontrollregion (GCR) bezeichnet wird. Die Hox-Gene, die der globalen Kontrollregion am nächsten liegen, werden am stärksten exprimiert. Diese Expression kehrt das ursprüngliche Muster der Hoxd10–13-Expression um, sodass Hoxd13 am stärksten exprimiert wird und sich am weitesten nach vorne erstreckt. Hoxd12, Hoxd11 und Hoxd10 werden in etwas engeren Bereichen exprimiert, sodass der vorderste Finger (z. B. der Daumen) Hoxd13, aber kein anderes Hox-Gen exprimiert. Somit trägt die erste Phase der Hoxd-Genexpression zur Spezifizierung der ZPA bei, während in der zweiten Phase die ZPA die Expressionsmuster der Hoxd-Gene vorgibt und diese Muster die Identität der Finger bestimmen.
Wie entstehen Handfläche und Handrücken (die Dorso-Ventral-Achse)?[8]
Die dorso-ventral-Achse der Gliedmaßen, also der z. B. Unterschied zwischen Hand- bzw. Fußrücken und Handfläche bzw. Fußsohle, wird durch das Ektoderm der Gliedmaßenknospe bestimmt.
Experimente haben gezeigt, dass wenn dieses Ektoderm um 180 Grad gedreht wird, sich die dorso-ventrale Achse umdreht, die Finger würden quasi auf dem Kopf stehen. Ein wichtiges Signalmolekül ist hierfür Wnt7a, welches nur im dorsalen Ektoderm der Gliedmaßenknospe gebildet wird. Wnt7a induziert die Aktivierung des Gens Lmx1b im dorsalen Mesenchym.
Wird Lmx1b in den ventralen Mesenchymzellen exprimiert, entwickeln diese Zellen einen dorsalen Phänotyp. Ähnlich führen Funktionsverlustmutationen im LMX1B-Gen beim Menschen zum Nagel-Patella-Syndrom; es werden also weder Nägel noch Kniescheiben ausgebildet. Umgekehrt markiert der Transkriptionsfaktor Engrailed-1 das ventrale Ektoderm der Gliedmaßenknospe und wird durch BMPs im darunter liegenden Mesoderm induziert.
Wnt7a wird zudem auch für die anterior-posteriore Achse benötigt, da Mäusen, denen dieses Gen fehlt, auch keine hinteren Finger aufweisen, weil ein Verlust von Wnt7a auch zu einer reduzierten Sonic hedgehog-Expression führt. Umgekehrt führt eine verstärkte Wnt7a-Signalübertragung im ventralen Ektoderm zu einem übermäßigen Wachstum der AER und zu zusätzlichen Zehen.
Wie werden die Finger „frei“?[9]
Am Ende der Musterbildung der Gliedmaßen sind BMPs dafür verantwortlich, dass die AER als auch die ZPA inaktiviert werden und zudem hemmen BMPs Wnt7 an der dorso-ventralen Achse. Das BMP-Signal eliminiert das Wachstum und die Musterbildung entlang aller drei Achsen. Was am Ende noch fehlt ist aber zu schauen, wie sich die Gelenke und die abgetrennten Finger bilden. Dies geschieht primär durch den programmierten Zelltod, der Apoptose.
Der Unterschied zwischen einem Hühnerfuß und dem Schwimmfuß einer Ente besteht im Vorhandensein oder Fehlen von Zelltod zwischen den Zehen. Nach einem bestimmten Stadium sterben die Zellen zwischen den Zehenknorpeln eines Kükens ab, selbst wenn sie in einen anderen Bereich des Embryos transplantiert gebracht werden. Zwischen dem Zeitpunkt, an dem der Zelltod festgelegt wird, und dem Zeitpunkt, an dem der Tod tatsächlich eintritt, nimmt die DNA-, RNA- und Proteinsynthese in der Zelle dramatisch ab.
Weitere Bereiche der Gliedmaßen, in denen der Zelltod eintritt betrifft die Trennung von Elle und Speiche, sowie zwischen den Gelenken.
Das Signal für die Apoptose im Autopodium wird von den BMP-Proteinen gegeben. BMP2, BMP4 und BMP7 werden jeweils im Bereich zwischen den Fingern exprimiert, und die Blockierung der BMP-Signalübertragung verhindert den Zelltod. Da diese BMPs im gesamten Bereich zwischen den Fingern exprimiert werden, wird angenommen, dass der Zelltod der Standardzustand wäre, wenn es keine aktive Unterdrückung der BMPs gäbe. Diese Unterdrückung erfolgt durch das Noggin-Protein, das im sich entwickelnden Knorpel der Finger bildet. Wenn Noggin im gesamten Gliedmaßenknospenbereich exprimiert wird, tritt keine Apoptose auf.
Interessanterweise wurden BMPs Knochen- und Knorpelgewebe nicht nur durch den Zelltod eliminieren, sondern sind auch an deren Bildung beteiligt.
Dieselben BMPs können je nach Vorgeschichte der reagierenden Zelle den Tod oder die Differenzierung induzieren. Diese Kontextabhängigkeit der Signalwirkung ist ein entscheidendes Konzept in der Entwicklungsbiologie. Sie ist auch für die Bildung von Gelenken von entscheidender Bedeutung. In frühen Stadien der Gliedmaßenknospe (vor der Knorpelverdichtung) konnte gezeigt werden, dass BMP2 und BMP7 einen Zelltod verursachen. Zwei Tage später bewirken dieselben Regionen, dass die Gliedmaßenknospenzellen Knorpel bilden. In einer sich normal entwickelnden Gliedmaße nutzen BMPs beide Eigenschaften, um Gelenke zu bilden.
Von Walen, Fledermäusen, Echsen und Kühen: Variationen im Bauplan[10]
Obwohl die Gliedmaßen von Wirbeltieren so unterschiedlich aussehen, bilden sie sich immer nach diesen vorgestellten Prinzipien und weisen dieselben zugrundliegenden Skelettelemente auf. Die große Bandbreite anatomischer Spezialisierungen in den Gliedmaßen, ist auf Veränderungen der Genexpression und unterschiedlichem Wachstum von Teilen der Gliedmaßen während der Embryonalentwicklung zurückzuführen. Dies ist ein hervorragendes Beispiel für die Modularität der Skelettelemente. Vergleicht man die Vordergliedmaße einer Fledermaus und eines Pferdes, so sieht man, dass beide zwar das Grundmuster der Gliedmaßenknochen beibehalten haben, die Gliedmaßen jedoch so verändert wurden, dass sie bei jedem Tier eine spezielle Funktion erfüllt. Bei der Fledermaus sind die Vordergliedmaßen an das Fliegen angepasst, und die Finger sind stark verlängert, um einen membranartigen Flügel zu stützen. Beim Pferd sind die Gliedmaßen an das Laufen angepasst, und die seitlichen Finger sind reduziert, der mittlere Mittelhandknochen ist verlängert, und Speiche und Elle sind für mehr Festigkeit miteinander verwachsen.
Wale und Delfine haben verlängerte Finger mit zusätzlichen Fingerliedern haben. Es wird vermutet, dass dies auf das Fortbestehen der AER zurückzuführen ist, der das Wachstum der Knospe verlängert. Im Gegensatz dazu hat sich bei den verlängerten Fingern der Fledermäuse, die den membranartigen Flügel stützen, die Anzahl der Fingerglieder nicht erhöht, sondern jedes Fingerglied ist länger.[11] Bei Fledermäusen gibt es bereits in einem sehr frühen Embryonalstadium Unterschiede in der Größe der Vorder- und Hinterbeine, obwohl die starke Verlängerung der Finger des Fledermausflügels relativ spät erfolgt, nachdem das Grundgerüst des Skeletts bereits festgelegt ist. Der Transkriptionsfaktor Prx1 wird in hoher Konzentration im Bereich der Fingerlieder des sich entwickelnden Fledermausflügels exprimiert, was möglicherweise zur Verlängerung der Finger beiträgt. Wenn der Enhancer aus dem Prx1-Gen der Maus durch den Prx1-Enhancer der Fledermaus ersetzt wird, kommt es zu einer geringen, aber signifikanten Verlängerung der Vordergliedmaßen der Maus. Die Verlängerung der Finger der Fledermausflügel könnte auch durch eine zweite Welle der Sonic Hedgehog-Signalübertragung gefördert werden. Eine erhöhte FGF-8-Produktion könnte das Auswachsen der Finger ebenfalls verlängern.[12]
Ein auffälliges Merkmal der Evolution der Gliedmaßen von Wirbeltieren ist, dass zwar eine Verringerung der Zehenanzahl häufig vorkommt, es jedoch keine modernen Arten mit mehr als fünf Zehen gibt. Der „Daumen” des Pandas, der wie eine sechste Zehe aussieht, ist in Wirklichkeit ein modifizierter Handgelenksknochen. Arten mit mehr als fünf Fingern kommen in den Fossilienfunden der frühesten Tetrapoden vor, wie beispielsweise Acanthostega, aber es ist nicht klar, ob es mehr als fünf morphologisch unterschiedliche Arten von Fingern gab. Bei heutigen Gliedmaßen mit Polydaktylie als Folge von Mutationen sind mindestens zwei der Finger gleich.[13]
In der Brustflosse von Zebrafischen wurden für bestimmte Hox-Gene vergleichbare Expressionsmuster entdeckt, die aus der Gliedmaßenentwicklung von Tetrapoden bekannt sind. Hox-Gene vom Zebrafisch wurden in einem Versuch in der Knospe der Maus exprimiert und zeigten dort Expressionsmuster zur Fingerentstehung. Änderungen in der Genregulation der Hox-Gene führten bei Zebrafischen zu einer Reduktion der Flossen. Mutationen der Gene „waslb“ und „vav2“ in den Flossen von Zebrafischen verstärken die Expression von Hox11-Genen, welche zur Bildung neuer Knochen, Muskeln und Gelenke bei diesen Fischen führen.[14] Eine Verringerung der Anzahl der Finger ist in der Evolution der Tetrapoden wiederholt aufgetreten. Bei den Gliedmaßen verschiedener Arten der australischen Skinkgattung Hemiergis, die eine unterschiedliche Anzahl von Fingern haben, korreliert eine verringerte Anzahl von Fingern mit einer Abnahme des Ausmaßes und der Dauer der Sonic Hedgehog-Signalübertragung.[15] Die Sonic Hedgehog-Signalübertragung ist auch in den frühen Gliedmaßenknospen von Rindern verändert, die als Paarhufer nur zwei Zehen haben.[16] Diese Veränderung in der Signalübertragung steht im Zusammenhang mit einer verringerten Expression des Gens Patched-1 (Ptch1), der für einen Rezeptor für Sonic Hedgehog codiert, das zur Zehenreduktion führt. Die Bindung von Sonic Hedgehog an Patched-1 beeinflusst auch, wie weit sich Sonic Hedgehog über die Gliedmaßenknospe ausbreiten kann. Da in den Gliedmaßenknospen von Rindern keine hohen Konzentrationen von Patched-1 vorhanden sind, breitet sich Sonic Hedgehog weiter über die Gliedmaßenknospe aus, was sich voraussichtlich auf die Anzahl und Art der sich entwickelnden Finger auswirkt.
Als die Schlange ihre Beine verlor[17]
Verschiedene Wirbeltiergruppen haben im Lauf der Evolution ihre Gliedmaßen reduziert, was besonders bei Schlangen charakteristisch ist. Fossile Schlangen aus der Kreidezeit hatten keine Vordergliedmaßen, aber noch relativ kleine Hintergliedmaßen, was darauf hindeutet, dass die Gliedmaßen bei Schlangen schrittweise reduziert wurden, beginnend mit den Vordergliedmaßen. Bei vielen heutigen Schlangen, darunter Kobras und Klapperschlangen, gibt es keine Anzeichen für die Bildung von Gliedmaßenknospen, und sowohl Vorder- als auch Hintergliedmaßen fehlen vollständig. Bei anderen, wie Pythons und Boas, gibt es kleine Knospen, die sich zu rudimentären Hintergliedmaßen entwickeln, die aus einem Beckengürtel und einem Femur mit einer Kralle bestehen. Die Tatsache, dass bei Embryonen heutiger Schlangen niemals Vordergliedmaßenknospen beobachtet wurden, lässt vermuten, dass der Verlust der Vorder- und Hintergliedmaßen während der Evolution durch unterschiedliche Mechanismen erfolgte. Die Kombination verschiedener Hoxgene im Seitenplattenmesoderms bestimmen die Position, an der sich Vordergliedmaßen entwickeln. Die weiter hinten liegenden Hox-Gene Hoxc8, Hoxc9 und Hoxc10 unterdrücken die Aktivität des Gens Tbx5, der die Identität der Vordergliedmaßenknospen bestimmt.
Bei Python-Embryonen wurde bisher nur die Verteilung des Hoxc8-Proteins untersucht; es wird entlang der gesamten Länge des Rumpfes exprimiert und schränkt damit die Tbx5-Expression vollständig ein, weswegen die Vordergliedmaßen sich nicht ausbilden. Der Verlust der Hintergliedmaßen ist aber eher mit der Regulation der Sonic-Hedgehog-Expression in der ZPA verbunden. Sonic Hedgehog wird in Pythonembryonen in den Hintergliedmaßen nur vorübergehend exprimiert, was zu rudimentären Hintergliedmaßen führt.
Die Analyse der Genome verschiedener Schlangen hat Mutationen in der ZPA identifiziert, wobei die Sequenzveränderungen bei vollständig gliedmaßenlosen Schlangen wie Kobras umfangreicher sind als bei Schlangen mit rudimentären Hintergliedmaßen wie Pythons. Transplantiert man die ZPA einer Schlange in die Gliedmaßenknospe von Mäuseembryonen unterbleibt die Sonic-Hedgehog-Expression und die sich anschließend entwickelnden Gliedmaßen der Maus sind stark verkürzt, ähnlich wie die Gliedmaßen von Mausembryonen, bei denen die ZPA komplett wurde. Diese Ergebnisse deuten darauf hin, dass der fortschreitende Verlust des ZPA der Evolution des Verlusts der Hintergliedmaßen bei Schlangen zugrunde liegt. Nur bei Pythons wird in der Frühphase der Entwicklung der Hintergliedmaßen vorübergehend Sonic Hedgehog exprimiert.
Warum sind die Hinterbeine im Laufe der Evolution nicht so leicht verloren gegangen wie die Vorderbeine? Ein möglicher Grund ist, dass die Entwicklung der Hinterbeine eng mit der Entwicklung der äußeren Genitalien verbunden ist. Diese unterschiedlichen Strukturen entstehen nicht nur aus benachbarten Zellpopulationen in Embryonen von Hühnern, Mäusen und Eidechsen, sondern ihre Entwicklung umfasst auch viele der gleichen Gene, so auch Sonic Hedgehog, deren Expression oft durch gemeinsame Kontrollregionen reguliert wird. Diese gemeinsame Nutzung von Kontrollregionen bedeutet, dass Mutationen in diesen Regionen die Entwicklung sowohl der Hinterbeine als auch der äußeren Genitalien beeinträchtigen könnten und daher weniger wahrscheinlich ausgewählt werden. Dazu mehr in einer späteren Episode.
Fische ohne Stacheln als Evolutionsbeleg[18]
Aber auch andere Gene sind an der Reduktion von Hintergliedmaßen beteiligt. Ein bekanntest Beispiel ist der Dreistachlige Stichling (Gasterosteus aculeatus), die morphologisch sehr vielfältig sind. Nach dem Rückgang der Gletscher der letzten Eiszeit eroberte der ursprünglich marine Fisch das Süßwasser. Durch die Eroberung von neuen Lebensräumen, unterteilbar in Fluss- und See-Habitate, mussten sie sich durch natürliche Selektion an neue Gegebenheiten wie Fressfeinde, Nahrungsangebot, Versteckmöglichkeiten und andere Habitatsveränderungen anpassen. Dies zeigt sich vor allem in der Variation der Lateralbeschildung, also einer Art Panzerung als Schutz vor Fressfeinden und ihrer Beckenstacheln, die modifizierte Hinterflossen sind.
Haben die Meeresformen des Stichlings zwei gute ausgebildete stachelige Hinterflossen, sind sie bei einigen Süßwasserpopulationen reduziert oder komplett verloren gegangen – inklusive des gesamten Beckengürtels. Der Selektionsmechanismus für diesen Verlust sind Raubfeinde im Süßgewässer, die im offenen Meer nicht vorkommen: Libellenlarven. Im offenen Gewässer tragen die Stacheln dazu bei, dass größere Raubfische den Stichling nicht so leicht fressen können. Am Gewässerboden von Teichen und Seen können aber Libellenlarven sich an den Stacheln junger Stichlinge festhalten und so als Beute fangen. Der Verlust der Stacheln wäre demnach für diese Fische ein Vorteil. Genetische Untersuchungen und Kreuzungsexperimente mit den Stichlingen haben gezeigt, dass eine mutierte Kontrollregion, des für die Identität der Hintergliedmaßen wichtigen Gens Pitx1, zum Verlust der Bauchstacheln und des Beckengürtels führt. Soll heißen: nicht das Gen Pitx1 ist mutiert, sondern einer seiner Schalter, dessen Mutation eine Expression in den Beinknospen blockiert.
Der Verlust der Bauchstacheln bei Stichlingen ist ein interessantes Beispiel für konvergente Evolution, da verschiedene Populationen unterschiedliche Mutationen in der Pitx1-Kontrollregion aufweisen, die in jeder Population unabhängig voneinander selektiert wurden.
Die wichtigsten Gene, die mit dem Verlust der Körperpanzerung und der Rückenflossen bei Süßwasser-Stichlingen in Verbindung stehen, wurden ebenfalls identifiziert. Der Verlust der Panzerung ist auf Mutationen in einem Schalter des Gens EDA zurückzuführen. EDA kodiert das Protein Ectodysplasin A, das bekanntermaßen für die normale Entwicklung der ektodermalen Organe bei Säugetieren unerlässlich ist. Mutationen in diesem Gen stehen im Zusammenhang mit hypohidrotischer ektodermaler Dysplasie beim Menschen, einer Erkrankung, bei der Haarfollikel, Zähne und andere ektodermale Strukturen sich nicht richtig entwickeln.
Die verminderte Entwicklung der Rückenstacheln des Stichlings wird durch eine Mutation verursacht, die zu einer Spleißveränderung im MSX2A-Gentranskript führt, was quantitative Unterschiede in der Anzahl der vollständigen und verkürzten Transkripte bei Meeres- und Süßwasserfischen zur Folge hat. MSX2A kodiert einen Transkriptionsfaktor, der an der normalen Entwicklung ektodermaler Organe und der Organregeneration bei Zebrafischen beteiligt ist. EDA und MSX2A befinden sich auf demselben Chromosom, was erklärt, warum der Verlust der Körperpanzerung und der Rückenstacheln zusammen auftreten.
Wie Insektenbeine unseren Beinen ähneln[19]
Werfen wir noch einen letzten Blick auf die Gliedmaßen einer völlig anderen Tiergruppe: den Arthropoden, zu denen Spinnen, Insekten und Krebstiere gehören. Natürlich sind die Beine der Arthropoden eine völlig andere Struktur, als die der Wirbeltiere. Und doch spielen in beiden Tierstämmen Hox-Gene eine wichtige Rolle bei der Identität ihrer Gliedmaßen.
Ein segmentierter Körper ist bei allen Embryonen von Arthropoden erkennbar, auch wenn bei einigen Klassen, wie beispielsweise den Spinnen, die segmentierte Struktur bei den adulten Tieren nicht leicht zu erkennen ist. Versuche, die Homologie verschiedener Segmenttypen zwischen den verschiedenen Gruppen von Gliederfüßern zu bestimmen und damit die Art der Veränderungen zu identifizieren, die während ihrer Evolution stattgefunden haben, haben sich allein aus anatomischen Gründen als schwierig erwiesen. Da Hox-Gene die Identität eines Segments vorschreiben, da sie die Expression bestimmter Zielgene, die die strukturellen Merkmale eines Segments festlegen, steuern, dann sollte die Veränderung der Segmentmorphologie eine Folge der Veränderungen des Expressionsmusters der Hox-Gene sein.
Wir konzentrieren uns hier auf Insekten und Krebstiere, bei denen am meisten über die Muster der Hox-Genexpression bekannt ist. Insekten und Krebstiere entwickelten sich aus einem Vorfahren, dessen Körper im Erwachsenenalter wahrscheinlich aus mehr oder weniger einheitlichen Segmenten bestand, die alle ähnliche paarige beinähnliche Fortsätze aufwiesen. Im Laufe der Evolution wurden die Beine auf bestimmte Segmente beschränkt.
Krebstiere eignen sich besonders gut für eine solche Untersuchung, da sie eine morphologische Vielfalt in ihrer Segmentierung aufweisen. Aber jedes Segment trägt eine von zwei Typen von Anhängseln: Laufbeine (die aber auch verschieden gestaltet sein können) oder spezialisierte „Fressbeine” (Maxillipeden), die in ihrer Struktur den Mundwerkzeugen ähneln und zur Manipulation von Nahrung dienen. Verschiedene Ordnungen von Krebstieren haben unterschiedliche Bein- und Maxillipeden-Ausstattungen am Thorax, und ein Vergleich der Muster der Hox-Genexpression bei verschiedenen Arten zeigt einen klaren Zusammenhang zwischen der Hox-Expression und der Segmentidentität und -funktion. Innerhalb der Malacostraca, den höheren Krebsen, mit acht Thoraxsegmenten, gibt es verschiedene Muster des Vorhandenseins von Maxilipeden und Laufbeinen im Thorax, also dem Burstabschnitt. Die Anzahl und Position der Maxillipeden auf den Thoraxsegmenten variiert zwischen verschiedenen Ordnungen der Malacostraca (z. B. Decapoda und Amphipoda), und ihr Vorkommen korreliert eindeutig mit der vorderen Grenze der Expression der Hox-Gene Ultrabithorax und Abdominal-A. Auch die anderen Hauptgruppen der Krebstiere zeigen die gleiche Korrelation zwischen dem Verlust der Ultrabithorax-Expression in einem Thoraxsegment und dem Vorhandensein eines Maxillipedes anstelle eines Beines. Das Vorhandensein von Maxillipeden an einem Segment ist immer mit einer fehlenden Ultrabithorax-Expression verbunden. Wird Ultrabithorax im Thorax exprimiert entstehen hingegen Laufbeine.
Dieser Kausalzusammenhang wurde auch experimentell überprüft, als man die zu den Flohkrebsen (Amphipoda) gehörenden Gattung Parhyale genetisch so manipulierte, dass bei einer Verringerung der Ultrabithorax-Expression anstelle von Laufbeinen maxilipedenähnliche Strukturen entstanden.
Bemerkenswert ist, dass die Transformationen nur die ersten drei Thoraxsegmente betrafen. Selbst wenn die Ultrabithorax-Expression im gesamten Thorax unterdrückt wurde, traten Maxillipeden nur an den ersten drei Segmenten auf; am vierten und den folgenden Thoraxsegmenten entwickelte sich wie üblich ein Laufbein. Dies spiegelt die natürliche Verteilung der Maxillipeden bei Krebstieren wider, da diese Gliedmaßen nicht weiter hinten als im Thoraxsegment 3 zu finden sind. In diesem Fall können wir daher mit Sicherheit sagen, dass Veränderungen in der Regulation von Ultrabithorax, die zu einer Veränderung seines räumlichen Expressionsmusters führten, die evolutionäre Veränderung bei Krebstieren vorangetrieben haben.
Trotz der enormen Vielfalt im Aussehen der heute lebenden Insekten sind ihre grundlegenden Körperbaupläne weniger vielfältig als die der Krebstiere. Alle erwachsenen Insekten haben nur drei Thoraxsegmente, die jeweils ein Beinpaar tragen. Flügel, sofern vorhanden, befinden sich am zweiten und dritten Segment oder, im Falle von Fliegen, nur am zweiten Segment, wobei der Flügel am dritten Thoraxsegment zu Halteren umgewandelt wurden, einem kleinen Organ, das während des Fluges für das Gleichgewicht sorgt.
Insektenfossilien weisen jedoch eine viel größere Vielfalt hinsichtlich der Position und Anzahl ihrer Beine und Flügel auf. Einige Insektenfossilien haben Anhängsel an jedem Segment, während andere nur in einem bestimmten Bereich des Thorax Beine haben. Die Anzahl der Abdominalsegmente mit Beinen variiert ebenso wie die Größe und Form der Beine. Flügel entstanden in der Evolution der Insekten später als Beine. Flügelähnliche Anhängsel sind bei einigen Insektenfossilien an allen Thorax- und Abdominalsegmenten vorhanden, bei anderen hingegen nur am Thorax. Um zu verstehen, wie diese unterschiedlichen Muster von Gliedmaßen im Laufe der Insektenevolution entstanden sein könnten, vergleichen wir zwei Ordnungen moderner Insekten, die Lepidoptera, also die Schmetterlinge und die Diptera, zu denen die Fliegen und Mücken gehören. Das Grundmuster der Hox-Genexpression entlang der anterior-posterioren Achse ist bei allen untersuchten heutigen Insektenarten ähnlich. Doch Schmetterlingslarven, also die Raupen, haben am Abdomen und Thorax zusätzlich kleine Gliedmaßen, die Protobeine und die adulten Tiere haben zwei Paar Flügel, während Fliegenlarven keine Beine am Abdomen haben und nur ein Paar Flügel im adulten Stadium. Inwiefern hängen diese Unterschiede mit den Unterschieden in der Hox-Genaktivität in den beiden Insektengruppen zusammen?
Verantwortlich für die Ausbildung der Beine ist das Gen Distal-less. Die Hoxgene des Boithorax-Komplexes, die im Hinterleib exprimiert werden unterdrücken bei Fliegen das Gen Distal-less und damit die Beinbildung im Abdomen. Wenn man den Bithorax-Komplex vollständig entfernt, trägt jedes Abdominalsegment im Fliegenembryo eine Beinscheibe und eine Flügelscheibe (diese Mutation ist aber letal, also tödlich, sodass sich keine Larven entwickeln). Dies deutet darauf hin, dass das Potenzial für die Entwicklung von Anhängseln in jedem Segment von Insekten, sogar bei den Fliegen, noch vorhanden ist und im Abdomen der Fliege aktiv unterdrückt wird. Dieser Beleg stützt die Annahme, dass die Vorfahren der Insekten Anhängsel an allen Segmenten hatten.
Während der Embryonalentwicklung von Schmetterlingen hingegen werden die Hox-Gene des Bithorax-Komplexes in den ventralen Teilen der embryonalen Abdominalsegmente ausgeschaltet; dies führt dazu, dass Distal-less exprimiert wird und sich Beinanhänge am Abdomen der Raupe entwickeln. Das Vorhandensein oder Fehlen von Beinen am Abdomen wird also dadurch bestimmt, ob bestimmte Hox-Gene dort exprimiert werden oder nicht, was ein weiterer Beleg dafür ist, dass Veränderungen im Muster der Hox-Genexpression eine Schlüsselrolle in der Evolution gespielt haben.
Dennoch dürften Unterschiede in den nachgeschalteten Zielen der Hox-Gene für die Evolution neuer Körperbaupläne noch wichtiger sein. Mitglieder des Bithorax-Komplexes unterdrücken die Entwicklung von Gliedmaßen im Hinterleib von Insekten, aber bei Krebstieren werden diese Gene im Brustkorb und im Hinterleib exprimiert, dennoch entwickeln sich Gliedmaßen, nämlich Laufbeine am Thorax und Schwimmbeine am Abdomen.
Der Unterschied muss in den Genen liegen, auf die die Gene der Bithorax-Gruppe bei Krebstieren und Insekten abzielen. Obwohl die Sequenz, die für die DNA-bindende Homöodomäne kodiert, zwischen den Hox-Genen verschiedener Arten hochkonserviert ist, haben die kodierenden Sequenzen außerhalb der Homöodomäne, die beeinflussen, mit welchen Genkontrollregionen und Genregulationsproteinen die Hox-Proteine interagieren können, im Laufe der Evolution erhebliche Veränderungen erfahren.
Evolutionäre Veränderungen in den Zielgenen der Hox-Gene helfen auch zu erklären, warum Fliegen zwei Flügel haben, während Schmetterlinge vier haben. Bei Fliegen bestimmt die Expression von Ultrabithorax im dritten Thoraxsegment (T3) die Ausbildung von Halteren, statt gewöhnlichen Flügeln. Im zweiten Segment wird Ultrabithorax zum Zeitpunkt der Flügelbildung nicht exprimiert und es bilden sich normale Flügel. Gene, von denen bekannt ist, dass sie an der Musterbildung des Flügels beteiligt sind, werden durch Ultrabithorax unterdrückt, weswegen es im dritten Segment zum Ausbleiben der Flügel kommt. Bei Schmetterlingen werden jedoch aufgrund von Veränderungen in den Kontrollregionen dieser Musterbildungsgene im Laufe der Evolution nur einige von ihnen durch Ultrabithorax unterdrückt, was zur Entwicklung eines Hinterflügels auf dem dritten Thorax-Segment führt.
Outro
Beine, ob nun bei Arthropoden, aber auch bei Wirbeltieren, sind eine wichtige Vorbedingungen für den Landgang. Doch um das Land zu erobern, reichte es nicht, nur laufen zu können – auch die Atmung musste sich grundlegend ändern. Im nächsten Video werfen wir daher einen genaueren Blick auf die Evolution der Lungenatmung: Welche Übergangsformen gab es, wie funktionierte die Sauerstoffaufnahme bei frühen Landwirbeltieren, und welche spannenden Einblicke liefern uns heutige Amphibien und Fische? Schaltet also wieder ein, wenn es heißt: Von Kiemen zu Lungen – der nächste große Schritt in der Evolution.
[1] Folgende Übersichtsliteratur für den gesamten Beitrag ist zu empfehlen:
- Baressi, MJF, Gilbert, SF (2020). Developmental Biology, Sinauer Associates. 12. Auflage. Kapitel 19 „Development of the Vertebrate Limb“ und Kapitel 25: „Development and Evolution“
- Carroll, SB et al. (2004). From DNA to diversity: molecular genetics and the evolution of animal design (2nd ed.). Malden, MA ; Wiley-Blackwell.
- Delaurier, A et al. (2008). The Mouse Limb Anatomy Atlas: an interactive 3D tool for studying embryonic limb patterning. BMC Dev. Biol. 8: 83–89. https://pubmed.ncbi.nlm.nih.gov/18793391/
- Hall, BK (2007). Fins into Limbs. The University of Chicago Press
- Wolpert, L. (2019): Principles of Development, Oxford University Press, 6. Auflage, Kapitel 10 „Organogenesis“ und Kapitel 14: „Evolution and Development“
- Zeller, R et al. (2009). Vertebrate limb bud development: moving towards integrative analysis of organogenesis. Nat Rev Genet 10, 845–858. https://doi.org/10.1038/nrg2681
[2] Siehe:
- Damon BJ, et al. (2008). Limb bud and flank mesoderm have distinct „physical phenotypes“ that may contribute to limb budding. Dev Biol. 321(2):319-30. https://pubmed.ncbi.nlm.nih.gov/18601915/
- Davey, MG et al. (2018). The chick limb: embryology, genetics and teratology. Int. J. Dev. Biol. 62: 85–95. https://pubmed.ncbi.nlm.nih.gov/29616743/
- Saunders, JW, et al. (1959). The differentiation of prospective thigh mesoderm grafted beneath the apical ectodermal ridge of the wing bud in the chick embryo. Dev. Biol. 1: 281–301. https://doi.org/10.1016/0012-1606(59)90030-2
- Tamura K, et al. (2008). The autopod: its formation during limb development. Dev Growth Differ. 50 Suppl 1:S177-87. https://pubmed.ncbi.nlm.nih.gov/18459983/
- Tickle, C (2017). An historical perspective on the pioneering experiments of John Saunders. Dev. Biol. 429: 374–381. https://pubmed.ncbi.nlm.nih.gov/28625869/
[3] Siehe:
- Brooke, NM et al. (1998). The ParaHox gene cluster is an evolutionary sister of the Hox gene cluster. Nature 392: 920–922. https://pubmed.ncbi.nlm.nih.gov/9582071/
- Davis, AP et al. (1995). Absence of radius and olna in mice lacking hoxa-11 and hoxd-11. Nature, 375, 791-795. https://pubmed.ncbi.nlm.nih.gov/7596412/
- Duboule, D (2007). The rise and fall of Hox gene clusters. Development 134: 2549–2560. https://pubmed.ncbi.nlm.nih.gov/17553908/
- Ferrier, DEK, Holland, PWH (2001). Ancient origin of the Hox gene cluster. Nat. Rev. Genet. 2: 33–34. https://pubmed.ncbi.nlm.nih.gov/11253066/
- Heffer, A, Pick, L (2013). Conservation and variation in Hox genes: how insect models pioneered the evo-devo field. Annual Reviews in Entomology, 58, 161-179. https://doi.org/10.1146/annurev-ento-120811-153601
- Holland, LZ et al. (2008). The amphioxus genome illuminates vertebrate origins and cephalochordate biology. Genome Res. 18: 1100–1111. https://pmc.ncbi.nlm.nih.gov/articles/PMC2493399/
- Pascual-Anaya, J et al. (2013). Evolution of Hox gene clusters in deuterostomes. BMC Dev. Biol. 13: 26. https://pubmed.ncbi.nlm.nih.gov/23819519/
[4] Siehe:
- Altabef, M et al. (1997). Dorso-ventral ectodermal compartments and origin of apical ectodermal ridge in developing chick limb. Development 124: 4547–4556 https://pubmed.ncbi.nlm.nih.gov/9409672/
- Cohn, MJ et al. (1995). Fibroblast growth factors induce additional limb development from the flank of chick embryos. Cell 80: 739–746. https://pubmed.ncbi.nlm.nih.gov/7889567/
- Cooper, KL et al. (2011). Initiation of proximo-distal patterning in the vertebrate limb by signals and growth. Science 332:1083–1086. https://pubmed.ncbi.nlm.nih.gov/21617075/
- DeLaurier, A et al. (2006). Pitx1 determines the morphology of muscle, tendon, and bones of the hindlimb. Dev. Biol. 299: 22–34. https://pubmed.ncbi.nlm.nih.gov/16989801/
- Lau, K et al. (2015). Anisotropic stress orients remodelling of mammalian limb bud ectoderm. Nat. Cell Biol. 17:569–579. https://www.nature.com/articles/ncb3156
- Minguillon, C et al. (2005). Tbx5 and Tbx4 are not sufficient to determine limb-specific morphologies but have common roles in initiating limb outgrowth. Dev. Cell 8:75–84. https://pubmed.ncbi.nlm.nih.gov/15621531/
- Nishimoto, S et al. (2014). A combination of activation and repression by a colinear Hox code controls forelimb-restricted expression of Tbx5 and reveals Hox protein specificity. PLoS Genet. 10: e1004245. https://pubmed.ncbi.nlm.nih.gov/24651482/
- Nishimoto, S, Logan, MP (2016). Subdivision of the lateral plate mesoderm and specification of the forelimb and hindlimb forming domains. Semin. Cell Dev. Biol. 49: 102–108. https://pubmed.ncbi.nlm.nih.gov/26643124/
- Rosello-Diez A, et al. (2011). Diffusible signals not autonomous mechanisms determine the main proximodistal limb subdivision. Science 332: 1086–1088. https://pubmed.ncbi.nlm.nih.gov/21617076/
- Saiz-Lopez, P et al. (2015). An intrinsic timer specifies distal structures of the vertebrate limb. Nature Commun. 6: 8108. https://pubmed.ncbi.nlm.nih.gov/26381580/
- Summerbell, D et al. (1973). Positional information in chick limb morphogenesis. Nature 244: 492–496. https://pubmed.ncbi.nlm.nih.gov/4621272/
- Tickle, C (2015). How the embryo makes a limb: determination, polarity and identity. J. Anat. 227:418–430. https://pubmed.ncbi.nlm.nih.gov/26249743/
- Zeller, R et al. (2009). Vertebrate limb bud development: moving towards integrative analysis of organogenesis. Nature Rev. Genet. 10: 845–858. https://pubmed.ncbi.nlm.nih.gov/19920852/
[5] Siehe:
- Bénazéraf, B et al. (2010). A random cell motility gradient downstream of FGF controls elongation of an amniote embryo. Nature 466: 248–252. https://pubmed.ncbi.nlm.nih.gov/20613841/
- Boehm, B et al. (2010). The role of spatially controlled cell proliferation in limb bud morphogenesis. PLoS Biol. 8:8e1000420. https://pubmed.ncbi.nlm.nih.gov/20644711/
- Fernandez-Teran, M, Ros, MA (2008). The apical ectodermal ridge: morphological aspects and signaling pathways. Int. J. Dev. Biol. 52: 857–871. https://pubmed.ncbi.nlm.nih.gov/18956316/
- Gros, J et al. (2010). Wnt5a/Jnk and FGF/Mapk pathways regulate the cellular events shaping the vertebrate limb. Curr. Biol. 20: 1993–2002. https://pubmed.ncbi.nlm.nih.gov/21055947/
- Gros, J, Tabin, CJ (2014). Vertebrate limb bud formation is initiated by localized epithelial-to-mesenchymal transition. Science 343:1253–1256. https://pmc.ncbi.nlm.nih.gov/articles/PMC4097009/
- Niswander, L et al. (1993). FGF-4 replaces the apical ectodermal ridge and directs outgrowth and patterning of the limb. Cell 75: 579–587. https://pubmed.ncbi.nlm.nih.gov/8221896/
- Verheyden, JM, Sun, X (2017). Embryology meets molecular biology: deciphering the apical ectodermal ridge. Dev. Biol. 429:387–390. https://pubmed.ncbi.nlm.nih.gov/28131856/
- Wyngaarden, LA et al. (2010). Oriented cell motility and division underlie early limb bud morphogenesis. Development 137: 2551–2558. https://pubmed.ncbi.nlm.nih.gov/20554720/
[6] Siehe:
- Bénazet, JD et al. (2009). A self-regulatory system of interlinked signaling feedback loops controls mouse limb patterning. Science 323:1050–1053. https://pubmed.ncbi.nlm.nih.gov/19229034/
- Dahn, RD, Fallon, JF (2000). Interdigital regulation of digit identity and homeotic transformation by modulated BMP signaling. Science 289:438–441. https://pubmed.ncbi.nlm.nih.gov/10903202/
- Harfe, BD et al. (2004). Evidence for an expansion-based temporal Shh gradient in specifying vertebrate digit identities. Cell 118:517–528. https://pubmed.ncbi.nlm.nih.gov/15315763/
- Hill, RE, Lettice, LA (2013). Alterations to the remote control of Shh gene expression cause congenital abnormalities. Trans. R. Soc. B 368:20120357. https://pmc.ncbi.nlm.nih.gov/articles/PMC3682722/
- Lettice, LA et al. (2008). Point mutations in a distant Shh cis-regulator generate a variable regulatory output responsible for preaxial polydactyly. Hum. Mol. Genet. 17:978–985 https://doi.org/10.1093/hmg/ddm370
- Lettice, LA et al. (2011). Enhancer-adoption as a mechanism of human developmental disease. Hum. Mutat. 32:1492–1499. https://doi.org/10.1002/humu.21615
- Litingtung, Y et al. (2002). Shh and Gli3 are dispensable for limb skeleton formation but regulate digit number and identity. Nature 418:979–983. https://pubmed.ncbi.nlm.nih.gov/12198547/
- Niswander, L et al. (1994). A positive feedback loop coordinates growth and patterning in the vertebrate limb. Nature 371:609–612. https://pubmed.ncbi.nlm.nih.gov/7935794/
- Pizette, S, Niswander, L (1999). BMPs negatively regulate structure and function of the limb apical ectodermal ridge. Development 126: 883–894. https://pubmed.ncbi.nlm.nih.gov/9927590/
- Riddle, RD et al. (1993). Sonic hedgehog mediates polarizing activity of the ZPA. Cell 175: 1401–1416. https://pubmed.ncbi.nlm.nih.gov/8269518/
- Suzuki, T et al. (2004). Tbx genes specify posterior digit identity through Shh and BMP signaling. Dev. Cell 6:43–53. https://pubmed.ncbi.nlm.nih.gov/14723846/
- Suzuki, T et al. (2008). Unique SMAD1/5/8 activity at the phalanx-forming region determines digit identity. Proc. Natl. Acad. Sci. USA 105:4185–4190 https://doi.org/10.1073/pnas.0707899105
- te Welscher, P et al. (2002). Progression of vertebrate limb development through SHH-mediated counteraction of GLI3. Science 298:827–830. https://pubmed.ncbi.nlm.nih.gov/12215652/
- Tickle, C. (2006). Making digit patterns in the vertebrate limb. Nat. Rev. Mol. Cell Biol. 7:1–9. https://pubmed.ncbi.nlm.nih.gov/16493412/
- Tickle, C, Towers, M (2017). Sonic hedgehog signaling in limb development. Front. Cell Dev. Biol. 5:14. https://pubmed.ncbi.nlm.nih.gov/28293554/
- Towers, M et al. (2008). Integration of growth and specification in chick wing digit-patterning. Nature 452:882–886. https://pubmed.ncbi.nlm.nih.gov/18354396/
- Vokes, SA et al. (2008). A genome-scale analysis of the cis-regulatory circuitry underlying Shh mediated patterning of the mammalian limb. Genes Dev. 22:2651–2663 https://pubmed.ncbi.nlm.nih.gov/18832070/
- Yang, Y et al. (1997). Relationship between dose, distance and time in Sonic Hedgehog-mediated regulation of anteroposterior polarity in the chick limb. Development 124: 4393–4404. https://pubmed.ncbi.nlm.nih.gov/9334287/
- Zeller, R et al. (2009). Vertebrate limb bud development: moving towards integrative analysis of organogenesis. Nature Rev. Genet. 10: 845–858. https://pubmed.ncbi.nlm.nih.gov/19920852/
[7] Siehe:
- Andrey, G et al. (2013). A switch between topological domains underlies HoxD genes collinearity in mouse limbs. Science 340:1234167 https://pubmed.ncbi.nlm.nih.gov/23744951/
- Goodman, FR (2002). Limb malformations and the human HOX genes. Am. J. Med. Genet. 112:256–265. https://pubmed.ncbi.nlm.nih.gov/12357469/
- Kmita, M et al. (2005). Early developmental arrest of mammalian limbs lacking HoxA/HoxD gene function. Nature 435:1113–1116. https://www.nature.com/articles/nature03648
- Nelson, CE et al. (1996). Analysis of Hox gene expression in the chick limb bud. Development 122: 1449–1466. https://pubmed.ncbi.nlm.nih.gov/8625833/
- Tanaka, M (2017). Evolution of vertebrate limb development. eLS 1–10. https://doi.org/10.1002/9780470015902.a0002099.pub2
- Wellik, DM, Capecchi, MR (2003). Hox10 and Hox11 genes are required to globally pattern the mammalian skeleton. Science 301: 363–367. https://pubmed.ncbi.nlm.nih.gov/12869760/
[8] Siehe:
- Arques, CG et al. (2007). Cell tracing reveals a dorsoventral lineage restriction plane in the mouse limb bud mesenchyme. Development 134: 3713–3722. https://pubmed.ncbi.nlm.nih.gov/17715176/
- Geduspan, JS, MacCabe, JA (1987). The ectodermal control of mesodermal patterns of differentiation in the developing chick wing. Dev. Biol. 124: 398–408 https://pubmed.ncbi.nlm.nih.gov/3678605/
- Riddle, RD et al. (1995). Induction of the LIM homeobox gene Lmx1 by Wnt-7a establishes dorsoventral pattern in the vertebrate limb. Cell 83: 631–640. https://pubmed.ncbi.nlm.nih.gov/7585966/
[9] Siehe:
- Garcia-Martinez, V et al. (1993). Internucleosomal DNA fragmentation and programmed cell death (apoptosis) in the interdigital tissue of the embryonic chick leg bud. J. Cell. Sci. 106: 201–208. https://pubmed.ncbi.nlm.nih.gov/8270624/
- Hartmann, C, Tabin, CJ (2001). Wnt-14 plays a pivotal role in inducing synovial joint formation in the developing appendicular skeleton. Cell 104: 341–351. https://pubmed.ncbi.nlm.nih.gov/11239392/
- Hernandez-Martinez, R, Covarrubias, L (2011). Interdigital cell death function and regulation: new insights on an old programmed cell death model. Dev. Growth Diff. 53: 245–258. https://pubmed.ncbi.nlm.nih.gov/21338350/
- Khan, IM et al. (2007). The development of synovial joints. Curr. Top. Dev. Biol. 79: 1–36. https://pubmed.ncbi.nlm.nih.gov/17498545/
- Kahn, J et al. (2009). Muscle contraction is necessary to maintain joint progenitor cell fate. Dev. Cell 16: 734–743. https://pubmed.ncbi.nlm.nih.gov/19460349/
- Koyama, E et al. (2008). A distinct cohort of progenitor cells participates in synovial joint and articular cartilage formation during mouse limb skeletogenesis. Dev. Biol. 316: 62–73. https://pubmed.ncbi.nlm.nih.gov/18295755/
- Lorda-Diez CI et al. (2015). Interdigital tissue regression in the developing limb of vertebrates. Int. J. Dev. Biol. 59: 55–62. https://pubmed.ncbi.nlm.nih.gov/26374526/
[10] Siehe:
- Boisvert, CA et al. (2008). The pectoral fin of Panderichthys and the origin of digits. Nature 456: 636–638. https://www.nature.com/articles/nature07339
- Gehrke, AR, Shubin, NH (2016). Cis-regulatory programs in the development and evolution of vertebrate paired appendages. Semin. Cell Dev. Biol. 57:31–39 https://pubmed.ncbi.nlm.nih.gov/26783722/
- Hoff, M (2014). A footnote to the evolution of digits. PLoS Biol. 12: e1001774. https://pmc.ncbi.nlm.nih.gov/articles/PMC3897374/
- Minguillon, C et al. (2009). Tbx4/5 gene duplication and the origin of vertebrate paired appendages. Proc. Natl Acad. Sci. USA 106: 21726–21730. https://pubmed.ncbi.nlm.nih.gov/19995988/
- Nakamura, T et al. (2016). Digits and fin rays share common developmental histories. Nature 537: 225–228. https://www.nature.com/articles/nature19322
- Onimaru, K et al. (2015). A shift in anterior-posterior positional information underlies the fin-to-limb evolution. eLife 4: e07048. https://pubmed.ncbi.nlm.nih.gov/26283004/
- Sordino, P et al. (1995). Hox gene expression in teleost fins and the origin of vertebrate digits. Nature 375: 678–681. https://pubmed.ncbi.nlm.nih.gov/7791900/
- Tanaka, M (2016). Fins into limbs: Autopod acquisition and anterior elements reduction by modifying gene networks involving 5’ Hox, Gli3, and Shh. Dev Biol. 413: 1–7 https://doi.org/10.1016/j.ydbio.2016.03.007
- Woltering, JM et al. (2014). Conservation and divergence of regulatory strategies at Hox loci and the origin of tetrapod digits. PLoS Biol. 12:e1001773. https://pubmed.ncbi.nlm.nih.gov/24465181/
[11] Richardson, MK, Oelschläger, HH (2002). Time, pattern, and heterochrony: a study of hyperphalangy in the dolphin embryo flipper. Evol Dev. 4: 435–444. https://pubmed.ncbi.nlm.nih.gov/12492144/
[12] Siehe:
- Cretekos C et al. (2008). Regulatory divergence modifies limb length between mammals. Genes & Dev. 22: 141-151 https://genesdev.cshlp.org/content/22/2/141
- Hockman, D et al. (2008). A second wave of Sonic hedgehog expression during the development of the bat limb. Proc. Natl Acad. Sci. USA. 105: 16982–16987. https://pubmed.ncbi.nlm.nih.gov/18957550/
[13] Jones, F (1939). The Thumb of the Giant Panda. Nature 143, 157. https://doi.org/10.1038/143157a0
[14] Hawkins et al. (2021). Latent developmental potential to form limb-like skeletal structures in zebrafish. Cell 184(4): 899-911 https://www.cell.com/cell/fulltext/S0092-8674(21)00003-9
[15] Shapiro, MD et al. (2003). Developmental basis of evolutionary digit loss in the Australian lizard Hemiergis. J.
Exp. Zool. B Mol. Dev. Evol. 297: 48–56. https://pubmed.ncbi.nlm.nih.gov/12955843/
[16] Siehe:
- Cooper, KL et al. (2014). Patterning and post-patterning modes of evolutionary digit loss in mammals. Nature 511: 41–45. https://pubmed.ncbi.nlm.nih.gov/24990742/
- Lopez-Rios, J. et al. (2014). Attenuated sensing of SHH by Ptch1 underlies evolution of bovine limbs. Nature 511: 46–51. https://pubmed.ncbi.nlm.nih.gov/24990743/
- Saxena, A et al. (2017). The origins, scaling and loss of tetrapod digits. Philos. Trans. R Soc. Lond. B Biol. Sci. 372: 20150482. https://pmc.ncbi.nlm.nih.gov/articles/PMC5182414/
[17] Siehe:
- Cohn, MJ, Tickle C (1999). Developmental basis of limblessness and axial patterning in snakes. Nature 399: 474–479. https://pubmed.ncbi.nlm.nih.gov/10365960/
- Infante, CR et al. (2015). Shared enhancer activity in the limbs and phallus and functional divergence of a limbgenital cis-regulatory element in snakes. Dev. Cell 35:107–119. https://pubmed.ncbi.nlm.nih.gov/26439399/
- Kvon, EZ et al. (2016). Progressive loss of function in a limb enhancer during snake evolution. Cell 167: 633–642. https://pubmed.ncbi.nlm.nih.gov/27768887/
- Leal, F, Cohn, MJ (2016). Loss and re-emergence of legs in snakes by modular evolution of Sonic hedgehog and HOXD enhancers. Curr. Biol. 26: 2966–2973 https://pubmed.ncbi.nlm.nih.gov/27773569/
- Leal, F, Cohn, MJ (2018). Developmental, genetic, and genomic insights into the evolutionary loss of limbs in snakes. Genesis 56: e23077. https://pubmed.ncbi.nlm.nih.gov/29095557/
[18] Siehe:
- Chan, YF et al. (2010). Adaptive evolution of pelvic reduction in sticklebacks by recurrent deletion of a Pitx1 enhancer. Science 327: 302–305. https://pubmed.ncbi.nlm.nih.gov/20007865/
- Colosimo, PF et al. (2005). Widespread parallel evolution in sticklebacks by repeated fixation of Ectodysplasin alleles.Science 307: 1928–1933. https://www.science.org/doi/10.1126/science.1107239
- Howes, TR et al. (2017). Dorsal spine evolution in threespine sticklebacks via a splicing change in MSX2A. BMC Biol. 15:115 https://pubmed.ncbi.nlm.nih.gov/29212540/
- Peichel, CL, Marques, DA (2017). The genetic and molecular architecture of phenotypic diversity in sticklebacks. Philos. Trans. R. Soc. Lond. B Biol. Sci. 372: 20150486. https://pmc.ncbi.nlm.nih.gov/articles/PMC5182418/
- Shapiro, MD et al. (2004). Genetic and developmental basis of evolutionary pelvic reduction in threespine sticklebacks. Nature 428: 717–723. https://pubmed.ncbi.nlm.nih.gov/15085123/
- Smith, C et al. (2021). Elevated temperatures drive the evolution of armour loss in the threespine stickleback Gasterosteus aculeatus. Functional Ecology, 35, 1735–1744. https://doi.org/10.1111/1365-2435.13846
[19] Siehe:
- Angelini, DR, Kaufman, TC (2005). Comparative developmental genetics and the evolution of arthropod body plans. Annu. Rev. Genet. 39: 95–119. https://pubmed.ncbi.nlm.nih.gov/16285854/
- Carroll, SB (1995). Homeotic genes and the evolution of arthropods and chordates. Nature 376: 479–485. https://pubmed.ncbi.nlm.nih.gov/7637779/
- Carroll, SB et al. (1995). Homeotic genes and the regulation and evolution of insect wing number. Nature 375: 58–61. https://pubmed.ncbi.nlm.nih.gov/7723843/
- Emerald, BS, Cohen, SM (2004). Spatial and temporal regulation of the homeotic selector gene Antennapedia is required for the establishment of leg identity in Drosophila. Dev. Biol. 267: 462–472. https://pubmed.ncbi.nlm.nih.gov/15013806/
- Estella, C et al. (2012). A dynamic network of morphogens and transcription factors patterns the fly leg. Curr. Top. Dev. Biol. 98: 173–198. https://pubmed.ncbi.nlm.nih.gov/22305163/
- Galindo, MI et al. (2002). Leg patterning driven by proximal-distal interactions and EGFR signaling. Science 297: 258–259. https://pubmed.ncbi.nlm.nih.gov/12114628/
- Heffer, A, Pick, L (2013). Conservation and variation in Hox genes: how insect models pioneered the evo-devo field. Annual Reviews in Entomology, 58, 161-179. https://doi.org/10.1146/annurev-ento-120811-153601
- Kojima, T. (2004). The mechanism of Drosophila leg development along the proximodistal axis. Dev. Growth Differ. 46: 115–129. https://pubmed.ncbi.nlm.nih.gov/15066191/
- Liubicich, DM et al. (2009). Knockdown of Parhyale Ultrabithorax recapitulates evolutionary changes in crustacean appendage morphology. Proc. Natl Acad. Sci. USA 106: 13892–13896. https://pubmed.ncbi.nlm.nih.gov/19666517/
- Martin, A et al. (2016). CRISPR/Cas9 mutagenesis reveals versatile roles of Hox genes in crustacean limb specification and evolution. Curr. Biol. 26: 14–26. https://pubmed.ncbi.nlm.nih.gov/26687626/
- Morata, G (2001). How Drosophila appendages develop. Nat. Rev. Mol. Cell Biol. 2: 89–97. https://pubmed.ncbi.nlm.nih.gov/11252967/
- Pavlopoulos, A, Akam, M (2011). Hox gene Ultrabithorax regulates distinct sets of target genes at successive stages of Drosophila haltere morphogenesis. Proc. Natl Acad. Sci. USA 108:2855–2860. https://pubmed.ncbi.nlm.nih.gov/21282633/
- Pavlopoulos, A et al. (2009). Probing the evolution of appendage specialization by Hox gene misexpression in an emerging model crustacean. Proc. Natl Acad. Sci. USA 106: 13897–13902. https://pubmed.ncbi.nlm.nih.gov/19666530/
- Si Dong, PD, et al. (2000). Coexpression of the homeobox genes Distal-less and homothorax determines Drosophila antennal identity. Development 127: 209–216. https://pubmed.ncbi.nlm.nih.gov/10603339/
- Weatherbee, SD, Carroll, S (1999). Selector genes and limb identity in arthropods and vertebrates. Cell 97: 283–286. https://pubmed.ncbi.nlm.nih.gov/10319808/
- Weatherbee, SD et al. (1999). Ultrabithorax function in butterfly wings and the evolution of insect wing patterns. Curr. Biol. 9: 109–115. https://pubmed.ncbi.nlm.nih.gov/10021383/