Text als pdf
Einführung
Die oxische Photosynthese gehört zu jenen autotrophen Stoffwechselreaktionen, die die Welt und die Evolution des Lebens am nachträglichen verändert haben. Mit Hilfe des Sonnenlichts können photosynthetisch aktive Lebewesen Wasser spalten und die daraus gewonnene Energie für die Herstellung von organischen Molekülen verwenden. Als Abfallprodukt der Wasserspaltung entsteht der freie Sauerstoff, welcher in die Ozeane und Atmosphäre entweicht (Grundlagenliteratur zur Photosynthese, siehe Munk 2008, 2018, Nelson & Cox 2010, Campbell et al. 2016, Kadereit et al. 2021, Madigan et al. 2020, Weiler et al. 2008, Alberts et al. 2024, Savada et al. 2019; Abb. 1). Die anoxische Variante der Photosynthese nutzt Schwefelwasserstoff statt Wasser (Bryant & Frigaard 2006, Bryant et al. 2007, Blankenship et al. 2007, Abb. 1). Und hier liegt das eigentlich Paradoxe: Wasser ist ein erstaunlich stabiles Molekül, seine Elektronen zu bekommen, um damit die Energie für die Produktion von organischen Molekülen zu nutzen ist deutlich schwieriger als bei Schwefelwasserstoff. Die einzigen Organismen, die in der Lage sind die oxische Photosynthese zu betreiben sind die Cyanobakterien (Abb. 2). In Pflanzenzellen wurden diese durch Endosymbiose zu den Chloroplasten. Das sind die winzigen grünen Strukturen, die sich in den Zellen aller Blätter befinden und diesen ihr eigenes Grün verleihen. Die Chloroplasten haben ihren Namen von dem Pigment, das ihnen ihre Farbe verleiht. Dabei handelt es sich um Chlorophyll, das für die Aufnahme der Sonnenenergie bei der Photosynthese verantwortlich ist. Das Chlorophyll ist in ein außergewöhnliches Membransystem eingebettet, das das Innere der Chloroplasten ausmacht. Dort findet das große Werk der Photosynthese statt: die Gewinnung von Elektronen aus dem Wasser.
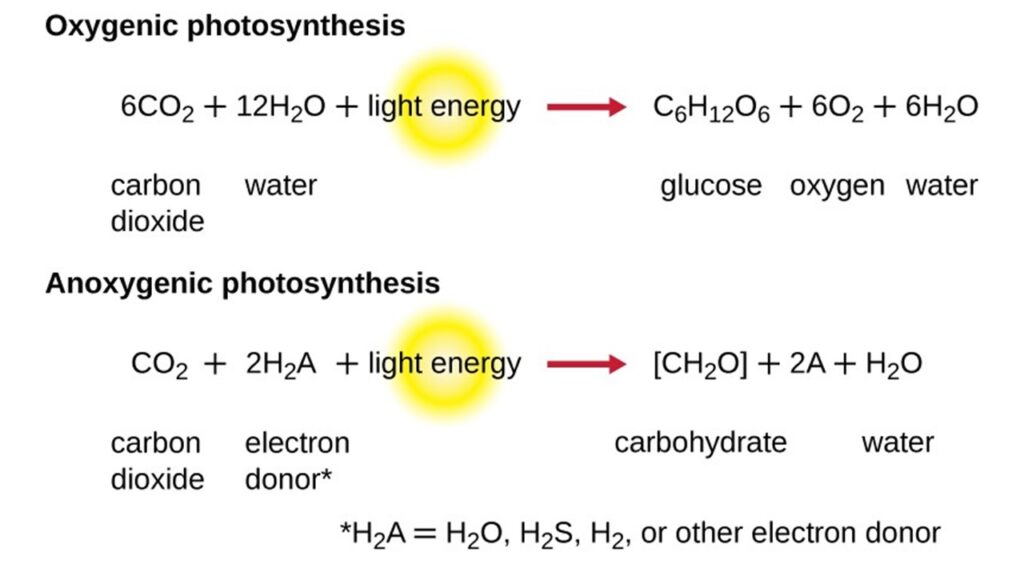
Abb. 1: oxische und anoxische Photosynthese
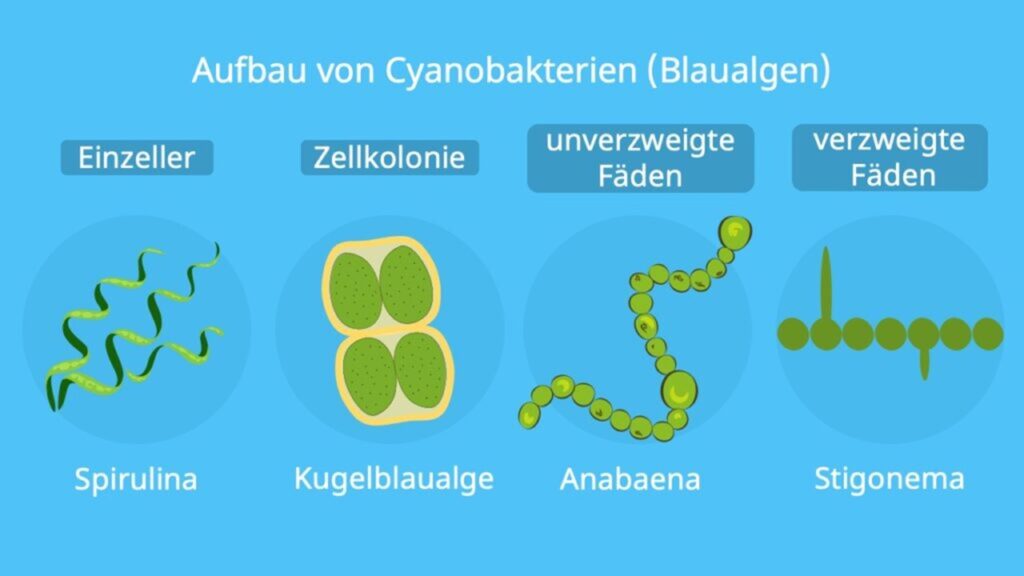
Abb. 2: Cyanobakterien
Die Lichtreaktion
Die Gewinnung von Elektronen aus Wasser ist zwar schwierig, aber die Pflanzen leisten dabei Außergewöhnliches. Die Komplexe aus Proteinen und Pigmenten sind molekular gesehen so groß, dass sie einer kleinen Stadt gleichkommen. Zusammen bilden sie zwei große Komplexe, die als Photosystem I und Photosystem II bekannt sind, und jeder Chloroplast enthält Tausende solcher Photosysteme. Ihre Aufgabe ist es, einen Lichtstrahl einzufangen und ihn in lebende Materie umzuwandeln. Um herauszufinden, wie sie das tun, brauchte man fast ein Jahrhundert und einige der elegantesten und raffiniertesten Experimente, die je durchgeführt wurden. Dies ist aber Stoff für adere Beiträge und wir konzentrieren uns darauf, was wir wissen.
Das konzeptionelle Herzstück der Photosynthese, der dem Ganzen einen Sinn gibt, ist als „Z-Schema“ bekannt, eine Formulierung, die Biochemiestudenten gleichermaßen fasziniert und erschreckt. Das Z-Schema wurde erstmals 1960 von Robin Hill aufgestellt und beschreibt das „Energieprofil“ der Fotosynthese (Hill 1937, 1939, Hill & Bendall 1960, Hill & Scarisbrick 1940, Hill & Whittingham 1953, Walker 2002a, b, Walker & Hill 1967, Blankenship 2014, Abb. 3). An erster Stelle stand dabei eine merkwürdige Frage der Thermodynamik. Es stellte sich heraus, dass die Photosynthese nicht nur neue organische Materie erzeugt, sondern auch ATP, die „Energiewährung“ des Lebens. Unerwarteterweise schienen diese beiden Faktoren immer miteinander verbunden zu sein: Je mehr organische Stoffe durch die Photosynthese erzeugt werden, desto mehr ATP wird produziert und umgekehrt. Die Sonne liefert offenbar zwei kostenlose Mittagessen im Gleichschritt. Das Z-Schema ist aber irreführend. Das Z sollte eigentlich um 90 Grad gedreht werden, um ein „N“ zu werden, dann würde es das Energieprofil der Photosynthese genauer wiedergeben. Stellt euch den ersten Aufwärtsstrich des „N“ als eine vertikale Aufwärtsreaktion vor: Es muss Energie zugeführt werden, damit es funktioniert. Der diagonale Abwärtshub des „N“ ist dann eine Abwärtsreaktion – dabei wird Energie freigesetzt, die in Form von ATP aufgefangen und gespeichert werden kann. Der abschließende Aufwärtshub ist wiederum eine Aufwärtsreaktion, bei der Energie zugeführt werden muss.
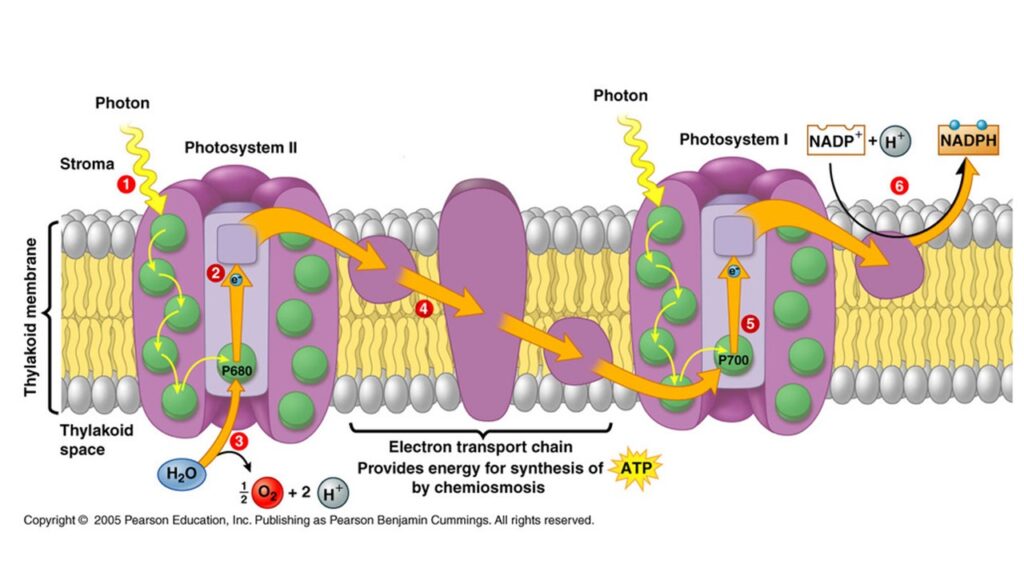
Abb. 3: Lichtreaktion
Bei der Photosynthese befinden sich die beiden Photosysteme – Photosystem I und II – an den beiden unteren Punkten des „N“. Ein Lichtphoton trifft auf das erste Photosystem und schleudert ein Elektron auf ein höheres Energieniveau; die Energie dieses Elektrons fällt dann in einer Reihe kleiner molekularer Schritte nach unten und liefert die Energie, die zur Herstellung von ATP benötigt wird. Wieder auf einem niedrigen Energieniveau angekommen, erreicht das Elektron das zweite Photosystem, wo ein zweites Photon es ein zweites Mal auf ein höheres Energieniveau katapultiert. Von diesem zweiten Hochpunkt aus wird das Elektron schließlich auf Kohlendioxid übertragen – der erste Schritt zur Herstellung von Zucker.
Das Z-Schema ist eine seltsam verworrene Vorgehensweise, aber es gibt gute technische Gründe dafür. Es grenzt an das chemisch Unmögliche, den Entzug von Elektronen aus Wasser mit der Umwandlung von Kohlendioxid in einen Zucker auf andere Weise zu verbinden. Der Grund dafür liegt in der Natur der Elektronenübertragung und insbesondere in der chemischen Affinität der Elektronen zu bestimmten Verbindungen. Wasser ist, wie wir gesehen haben, sehr stabil: Es hat eine hohe Affinität zu seinen Elektronen. Um dem Wasser ein Elektron zu entreißen, bedarf es einer enormen Anziehungskraft, d. h. eines sehr starken Oxidationsmittels. Dieses starke Oxidationsmittel ist eine gefräßige Form von Chlorophyll, die sich durch die Absorption von energiereichen Photonen verwandelt. Aber ein Molekül, das Elektronen fest umklammert, ist chemisch gesehen nicht geneigt, sie wegzustoßen. So ist es auch mit dieser Form des Chlorophylls. Wenn es durch Licht aktiviert wird, hat es eine enorme Kraft, um Elektronen aus dem Wasser zu ziehen, aber wenig Kraft, um sie anderswo wegzustoßen. Im Fachjargon ist es ein starkes Oxidationsmittel, aber ein schwaches Reduktionsmittel.
Bei Kohlendioxid stellt sich das umgekehrte Problem. Es ist ebenfalls sehr stabil und hat kein chemisches Verlangen danach, mit weiteren Elektronen vollgestopft zu werden. Es wird nur zähneknirschend Elektronen von einem sehr starken Reduktionsmittel aufnehmen. Dies erfordert eine andere Form von Chlorophyll: Wenn es durch Licht aktiviert wird, hat diese Form des Chlorophylls die Macht, seine Elektronen auf ein anderes Molekül zu schieben, das sie ebenfalls loswerden will, nämlich auf NADPH, und schließlich auf Kohlendioxid.
Es gibt also einen Grund für zwei Photosysteme in der Photosynthese. Das ist keine wirkliche Überraschung. Die schwierigere Frage ist jedoch: Wie konnte sich ein so komplexes, miteinander verbundenes System entwickeln? Diese Sequenz besteht eigentlich aus fünf Teilen. Der erste Teil ist der „sauerstoffentwickelnde Komplex“, eine Art molekularer Nussknacker, der die Wassermoleküle so positioniert, dass ihre Elektronen nacheinander herausgesprengt werden und Sauerstoff als Abfallprodukt freigesetzt wird. Dann kommt das Photosystem II, das sich bei Aktivierung durch Licht dem sauerstoffentwickelnden Komplex diese Elektronen entreißt. Dann folgt eine Elektronentransportkette, die die Elektronen weiterleitet. Die Elektronentransportkette nutzt das abwärts gerichtete Energiegefälle, um ein wenig ATP herzustellen, bevor sie dieselben Elektronen an das Photosystem I abgibt. Hier werden sie durch ein weiteres Photon wieder auf ein hohes Energieniveau gebracht, wo sie von NADPH festgehalten werden, einem starken Elektronenschieber, der nichts lieber möchte, als sie wieder loszuwerden. Und dann kommt die molekulare Maschinerie, die benötigt wird, um Kohlendioxid zu aktivieren und in Zucker umzuwandeln.
Mit Hilfe des NADPH, der vom Photosystem I erzeugt wird, wird die Umwandlung von Kohlendioxid in Zucker durch Chemie und nicht durch Licht angetrieben und ist als Dunkelreaktion bekannt. Diese fünf Systeme arbeiten nacheinander, um dem Wasser Elektronen zu entziehen und sie auf Kohlendioxid zu übertragen. Es ist eine enorm komplizierte Art, eine Nuss zu knacken, aber es scheint die einzige Möglichkeit zu sein, diese spezielle Nuss zu knacken. Die große evolutionäre Frage ist, wie all diese komplexen, miteinander verbundenen Systeme entstanden sind und auf genau die richtige Art und Weise, vielleicht sogar auf die einzige Art und Weise, organisiert wurden, um die sauerstoffhaltige Photosynthese funktioniert?
Evolution der Photosysteme
Tatsache ist, dass sich die oxische Photosynthese nur einmal entwickelt hat. Der Sitz der Photosynthese, der Chloroplast, befindet sich in allen photosynthetischen Zellen aller Pflanzen und Algen. Chloroplasten sind allgegenwärtig und offensichtlich miteinander verwandt. Sie teilen eine geheime Geschichte. Der Hinweis auf ihre Vergangenheit liegt in ihrer Größe und Form: Sie sehen aus wie kleine Bakterien, die im Inneren einer größeren Wirtszelle leben. Dieser Hinweis auf bakterielle Abstammung wird durch die Existenz unabhängiger DNA-Ringe in allen Chloroplasten bestätigt. Diese DNA-Ringe werden bei jeder Teilung der Chloroplasten kopiert und an die Töchter weitergegeben, genau wie bei Bakterien. Die detaillierte Abfolge der Buchstaben in der Chloroplasten-DNA bestätigt nicht nur die Verbindung zu den Bakterien, sondern zeigt auch mit dem Finger auf den nächsten lebenden Verwandten: die Cyanobakterien. Nicht zuletzt ist das Z-Schema der pflanzlichen Photosynthese mit all seinen fünf Bestandteilen in den Cyanobakterien genau wiederzufinden (wenn auch mit einfacheren Maschinen). Kurzum, es besteht kein Zweifel daran, dass die Chloroplasten einst freilebende Cyanobakterien waren. Die Cyanobakterien, einst fälschlicherweise als „Blaualgen“ bezeichnet, sind die einzige bekannte Gruppe von Bakterien, die über die „sauerstoffhaltige“ Form der Photosynthese Wasser spalten können. Wie es dazu kam, dass einige von ihnen in einer größeren Wirtszelle lebten, ist ein Rätsel, das in die Tiefen der geologischen Zeit eingewickelt ist. Zweifellos geschah es vor mehr als 1.000 Millionen Jahren, aber vermutlich wurden sie eines Tages einfach verschlungen, überlebten die Verdauung und erwiesen sich schließlich als nützlich für ihre Wirtszelle. Der mit Cyanobakterien imprägnierte Wirt gründete daraufhin zwei große Reiche, die Algen und die Pflanzen, die sich heute alle durch ihre Fähigkeit definieren, von Sonne und Wasser zu leben, und zwar mit Hilfe des Photosyntheseapparats, den sie von ihren bakteriellen Gästen geerbt haben (zur Endosymbiontentheorie siehe Margulis 1967, 1970, Margulis & Bermudes 1985, Margulis & Sagan 1997, McFadden 2001, Gould et al. 2008, Turner et al. 1999, Martin et al. 2015).
Der beste Weg, sich die Ursprünge der Photosynthese näher anzuschauen ist die Untersuchung ihrer Gene und ihrer physikalischen Strukturen, insbesondere in ihren Proteinstrukturen. In den letzten zwei oder drei Jahrzehnten wurden die detaillierten molekularen Strukturen sowohl pflanzlicher als auch bakterieller Photosysteme eingehend untersucht, wobei die Wissenschaftler eine ganze Reihe von Techniken einsetzten, deren Namen für nicht minder schwierige Methoden stehen, von der Röntgenkristallographie bis zur Elektronen-Spin-Resonanz-Spektroskopie. Wie diese Techniken funktionieren, braucht uns hier nicht zu interessieren; es genügt zu wissen, dass sie eingesetzt wurden, um die Formen und Strukturen der photosynthetischen Komplexe in fast atomarer Auflösung darzustellen. Die Architektur z. B. der über 46.000 Atome des Photosystems II sind im Wesentlichen geklärt – es gibt nur Detaildiskussionen um die genaueren Positionen einer Handvoll kritischer Atome des wasserspaltenden Komplexes.
Im Jahr 2006 wies ein Team unter der Leitung von Bob Blankenship nach, dass die beiden Photosysteme in Bakterien außerordentlich gut konserviert sind (Sadekar et al. 2006). Trotz der enormen evolutionären Abstände zwischen den verschiedenen Bakteriengruppen sind die Kernstrukturen der Photosysteme nahezu identisch, so dass sie mit einem Computer im Raum übereinandergelegt werden können. Darüber hinaus bestätigte Blankenship eine weitere Verbindung, die Forscher schon lange vermutet hatten: Die beiden Photosysteme haben ebenfalls eine gemeinsame Kernstruktur und sind mit ziemlicher Sicherheit vor langer, langer Zeit aus einem gemeinsamen Vorfahren hervorgegangen. Mit anderen Worten: Es gab einmal ein einziges Photosystem. Irgendwann wurde das Gen dupliziert, so dass zwei identische Photosysteme entstanden. Diese haben sich unter dem Einfluss der natürlichen Selektion langsam voneinander entfernt, wobei sie sich strukturell sehr ähnlich sind. Schließlich wurden die beiden Photosysteme im Z-Schema der Cyanobakterien aneinandergekoppelt und später in den Chloroplasten an die Pflanzen und Algen weitergegeben. Hinter dieser einfachen Erzählung verbirgt sich jedoch ein faszinierendes Dilemma.
Die Duplizierung eines primitiven Photosystems könnte das Problem der sauerstoffhaltigen Photosynthese niemals lösen – es könnte niemals einen starken Zug mit einem starken Schub von Elektronen verbinden. Bevor die Photosynthese funktionieren konnte, mussten die beiden Photosysteme in entgegengesetzte Richtungen divergieren, und erst dann konnten sie sinnvoll miteinander verknüpft werden. Es stellt sich also die Frage, welche Abfolge von Ereignissen sie auseinandertreiben könnte, um sie dann wieder als vertraute, aber gegensätzliche Partner zu verbinden? Der beste Weg, die Antwort zu finden, ist ein Blick auf die Photosysteme selbst (zur Struktur der Photosysteme siehe: Sadekar et al. 2006, Golbeck 1987, Subin et al. 1986, Rutherford & Heathcote 1985, Yamori & Shikanai 2016, Nelson & Yocum 2006, Hope 2000, Loll et al. 2005, Okubo et al. 2007, Guskov et al. 2009, Cox et al. 2020, Zouni et al. 2001, Ferreira et al. 2004; zur Evolution der Photosysteme, die im Folgenden zusammengefasst wird, siehe: Sadekar et al. 2006, Orf et al. 2018, Oliver et al. 2023, Cardona 2015, 2017, 2018, 2019, Cardona & Rutherford 2019, Cardona et al. 2019 Lockau & Nitschke 1993, Rutherford & Faller 2003, Martin et al. 2017, Allen 2005, Allen & Martin 2007, Hohmann-Marriott & Blankenship 2011, Raymond et al. 2002). Diese sind im Z-Schema der Cyanobakterien vereint, haben aber ansonsten eine interessant abweichende Evolutionsgeschichte. Lassen wir einmal beiseite, woher die Photosysteme ursprünglich stammen, und werfen wir einen kurzen Blick auf ihre heutige Verbreitung in der Welt der Bakterien (Abb. 4). Abgesehen von den Cyanobakterien sind sie nie gemeinsam in einem Bakterium zu finden. Einige Bakteriengruppen verfügen nur über das Photosystem I, andere nur über das Photosystem II. Jedes Photosystem arbeitet für sich, um unterschiedliche Ziele zu erreichen, und ihre genauen Aufgaben geben einen erstaunlichen Einblick in die Entwicklung der sauerstoffhaltigen Photosynthese. In Bakterien erfüllt das Photosystem I genau dieselbe Aufgabe wie in Pflanzen. Es nimmt Elektronen aus einer anorganischen Quelle auf und gibt diese an das NADPH weiter, der sie an Kohlendioxid weitergibt, um Zucker herzustellen. Der Unterschied liegt in der anorganischen Quelle der Elektronen. Anstelle von Wasser, mit dem es überhaupt nicht umgehen kann, bezieht das Photosystem I Elektronen aus Schwefelwasserstoff oder Eisen, die beide viel leichter zu handhaben sind als Wasser. Das von Photosystem I gebildete NADPH kann übrigens auch auf rein chemischem Wege gebildet werden, zum Beispiel in den hydrothermalen Schloten. Auch hier wird NADPH verwendet, um Kohlendioxid über eine ähnliche Reihe von Reaktionen in Zucker umzuwandeln. Die einzige wirkliche Neuerung des Photosystems I bestand also darin, Licht für eine Aufgabe zu nutzen, die zuvor allein durch Chemie erledigt wurde.
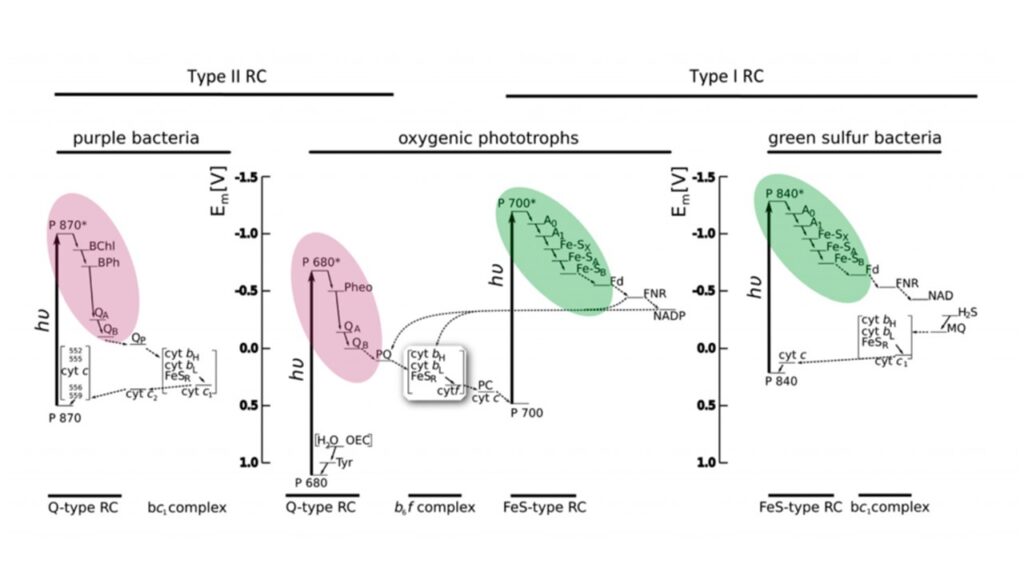
Abb. 4: In welchen Bakterien kommen die Photosysteme vor?
An dieser Stelle sei auch angemerkt, dass die Fähigkeit, Licht in Chemie umzuwandeln, nichts Besonderes ist: Fast jedes Pigment kann dies (Mauzerall 1998). Die chemischen Bindungen in Pigmenten sind gut darin, Lichtphotonen zu absorbieren. Dabei wird ein Elektron auf ein höheres Energieniveau angehoben, und nahe gelegene Moleküle können es leicht einfangen. Infolgedessen wird das Pigment photooxidiert: Es braucht ein Elektron, um die Bilanz auszugleichen, und nimmt es aus Eisen oder Schwefelwasserstoff auf. Das ist alles, was Chlorophyll tut. Chlorophyll ist ein Porphyrin, das in seiner Struktur dem Häm nicht unähnlich ist, dem Pigment, das den Sauerstoff in unserem Blut transportiert. Viele andere Porphyrine können ähnliche Tricks mit Licht ausführen. Entscheidend ist, dass Porphyrine zu den komplexeren Molekülen gehören, die aus Asteroiden isoliert und im Labor unter plausiblen präbiotischen Bedingungen synthetisiert wurden. Mit anderen Worten: Porphyrine hätten sich höchstwahrscheinlich spontan auf der frühen Erde gebildet.
Kurz gesagt, das Photosystem I nahm ein einfaches Pigment, ein Porphyrin, und koppelte seine spontane lichtgesteuerte Chemie mit Reaktionen, die ohnehin in Bakterienzellen ablaufen. Das Ergebnis war eine primitive Form der Photosynthese, die das Licht nutzen konnte, um Elektronen aus „einfachen“ Quellen wie Eisen und Schwefelwasserstoff abzuziehen und die Elektronen an Kohlendioxid weiterzugeben, um Zucker zu bilden. Diese Bakterien nutzen also Licht, um Nahrung zu erzeugen.
Was ist mit Photosystem II? Die Bakterien, die dieses Photosystem verwenden, nutzen das Licht, um einen ganz anderen Trick zu vollbringen. Bei dieser Form der Photosynthese wird keine organische Materie erzeugt. Vielmehr wird die Lichtenergie in chemische Energie, ja sogar in Elektrizität, umgewandelt, die zum Antrieb der Zelle verwendet werden kann. Der Mechanismus ist sehr einfach. Wenn ein Photon auf ein Chlorophyllmolekül trifft, wird ein Elektron wie zuvor auf ein höheres Energieniveau hochgezappt, wo es von einem nahegelegenen Molekül eingefangen wird. Dieses Elektron wird dann in einer Elektronentransportkette von Träger zu Träger weitergereicht, wobei jedes Mal ein wenig Energie freigesetzt wird, bis es wieder auf ein niedriges Energieniveau zurückgekehrt ist. Ein Teil der dabei freigesetzten Energie wird aufgefangen, um ATP herzustellen. Schließlich wird das erschöpfte Elektron zum gleichen Chlorophyll zurückgebracht, von dem es ausgegangen ist, und der Kreislauf ist geschlossen. Kurz gesagt, das Licht bringt ein Elektron auf ein hohes Energieniveau, und während es in einer Kaskade auf ein „ruhendes“ Niveau zurückfällt, wird die freigesetzte Energie als ATP aufgefangen, eine Energieform, die die Zelle nutzen kann. Es ist einfach ein lichtbetriebener Stromkreis.
Wie ist ein solcher Stromkreis entstanden? Auch hier lautet die Antwort: durch Mischung und Anpassung. Die Elektronentransportkette ist mehr oder weniger dieselbe wie die für die Atmung, die sich ebenfalls in den Schloten entwickelt hat; sie wurde nur für einen etwas anderen Zweck ausgeliehen. Wie wir bereits festgestellt haben, werden bei der Atmung Elektronen aus der Nahrung entnommen und schließlich an Sauerstoff weitergegeben, um Wasser zu bilden. Nebenbei ist auch die Atmung nicht zwingend an Sauerstoff gebunden. Es gibt nämlich auch Formen der anaeroben Atmung, bei der die Elektronen dann nicht an Sauerstoff, sondern an andere Moleküle weitergegeben werden (z. B. NO3–, NO2–, SO42–, S, CO32– [CO2], FeIII; Madigan et al. 2020). Die freigesetzte Energie wird zur Erzeugung von ATP verwendet. Bei dieser Form der Photosynthese geschieht genau das Gleiche: Hochenergetische Elektronen werden entlang einer Kette nicht an Sauerstoff, sondern an eine „greifende“ (oxidierende) Form des Chlorophylls abgegeben. Je mehr das Chlorophyll Elektronen „ziehen“ kann (d. h. je näher es dem Sauerstoff in seiner chemischen Beschaffenheit ist), desto effizienter ist die Kette, die die Elektronen ansaugt und ihnen ihre Energie entzieht. Der große Vorteil ist, dass kein Treibstoff oder Nahrung benötigt wird, zumindest nicht für die Bereitstellung von Energie.
Generell lässt sich also sagen, dass die einfacheren Formen der Photosynthese einen mosaikartigen Charakter haben. Bei beiden Formen wird ein neuer Wandler, das Chlorophyll, in eine bestehende molekulare Maschinerie eingebaut. In einem Fall wandelt diese Maschinerie Kohlendioxid in Zucker um, im anderen Fall produziert sie ATP. Was das Chlorophyll betrifft, so bildeten sich ähnliche Porphyrinpigmente wahrscheinlich spontan auf der frühen Erde, und die natürliche Auslese erledigte den Rest. In jedem Fall verändern kleine Veränderungen in der Struktur des Chlorophylls die Wellenlänge des absorbierten Lichts und damit die chemischen Eigenschaften.
Ursprünge des Z-Schemas
Die offene Frage: Wie wurde das alles im Z-Schema der Cyanobakterien miteinander verknüpft, um den ultimativen Brennstoff, das Wasser, zu spalten? Die kurze Antwort lautet: Wir wissen es nicht genau. Es gibt Möglichkeiten, eine eindeutige Antwort zu finden, aber leider haben sie nicht funktioniert. Wir können zum Beispiel die Gene für die Photosysteme in Bakterien systematisch vergleichen und gegenüberstellen, um einen Genbaum zu erstellen, der die Abstammung der Photosysteme verrät. Solche Bäume werden jedoch durch eine Tatsache des bakteriellen Lebens – dem horizontalen Gentransfer – gefällt. Diesen haben wir in einigen vorherigen Episoden kennengelernt. Er horizontaler Gentransfer ermöglicht den Austausch von genetischem Material zwischen verschiedenen Bakterienarten in einer Generation. Bakterien werfen mit ihren Genen um sich, ohne Rücksicht auf die Arbeit der Genetiker. Das Ergebnis ist eher ein Netz als ein Baum, in dem die Gene einiger Bakterien in anderen, völlig unverwandten Bakterien landen. Und das bedeutet, dass wir keinen wirklichen genetischen Beweis dafür haben, wie die Photosysteme nach dem Z-Schema zusammengebaut worden sind. Das heißt aber nicht, dass wir die Antwort nicht herausfinden können. Hier soll die Hypothese des britischen Biochemikers John Allen vorgestellt werden (Martin et al. 2017, Allen 2005, Allen & Martin 2007, siehe auch Sanchez-Baracaldo & Cardona 2020, Mulkidjanian et al. 2006, Soo et al. 2017, Abb. 5).
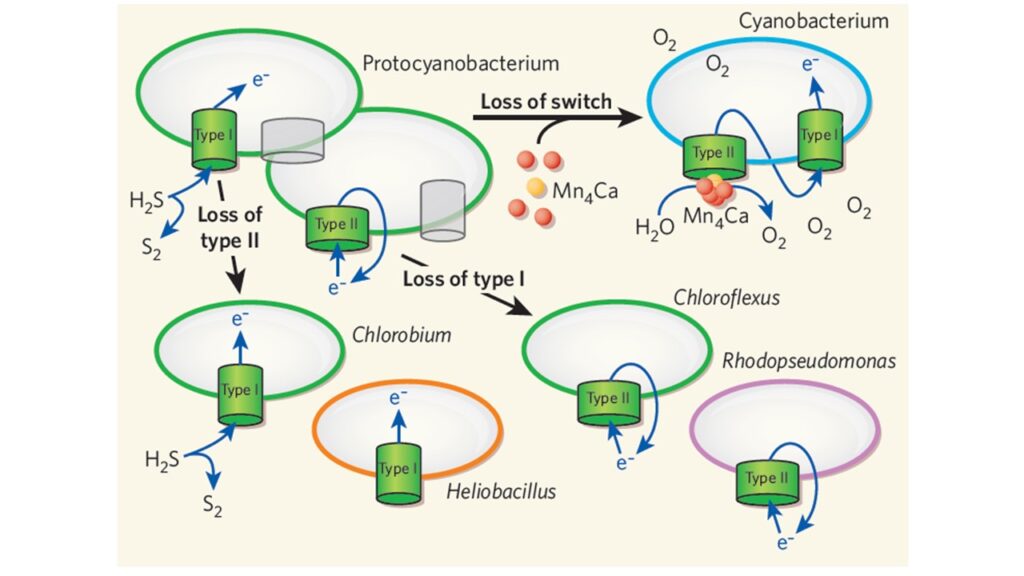
Abb. 5: Evolution der Photosysteme
Viele Bakterien schalten ihre Gene als Reaktion auf Veränderungen in ihrer Umgebung ein und aus; das ist an sich schon eine Binsenweisheit. Einer der wichtigsten Umweltschalter ist das Vorhandensein oder Fehlen von Rohstoffen. Im Großen und Ganzen verschwenden Bakterien keine Energie mit dem Aufbau neuer Proteine zur Verarbeitung von Rohstoffen, wenn keine vorhanden sind; sie stellen die Arbeit einfach bis auf weiteres ein. Rohstoffknappheit kann z. B. in schwankenden Umgebungen vorkommen – vielleicht einen Stromatolithen in flachen Meeren, in der Nähe eines hydrothermalen Schlots, der Schwefelwasserstoff in die Welt abgibt. Die Bedingungen würden je nach Gezeiten, Strömungen, Jahreszeit, hydrothermaler Aktivität und so weiter variieren. Entscheidend ist, dass Allens hypothetisches Bakterium beide Photosysteme besitzt, so wie die heutigen Cyanobakterien, aber im Gegensatz zu diesen immer nur eines davon gleichzeitig nutzt. Wenn Schwefelwasserstoff vorhanden ist, schalten die Bakterien das Photosystem I ein und nutzen es, um aus Kohlendioxid organische Stoffe zu erzeugen. Sie können diese neue Materie aufnehmen, um zu wachsen, sich fortzupflanzen und so weiter. Wenn sich jedoch die Bedingungen ändern und die Stromatolithen keine Rohstoffe mehr haben, schalten diese Bakterien auf Photosystem II um. Jetzt geben sie die Produktion neuer organischer Stoffe auf (sie wachsen und vermehren sich nicht mehr), aber sie können sich selbst erhalten, indem sie das Sonnenlicht nutzen, um direkt ATP herzustellen, bis bessere Zeiten kommen. Jedes Photosystem hat seinen eigenen Nutzen, und jedes hat sich, wie wir gesehen haben, in einer Reihe von einfachen Schritten entwickelt. Was aber passiert, wenn ein hydrothermaler Schlot abstirbt oder wechselnde Strömungen zu langwierigen Veränderungen in der Umwelt führen? Die Bakterien müssen sich nun die meiste Zeit auf den Elektronenkreislauf des Photosystems II verlassen.
Das Problem besteht hier, dass mit der Zeit der Kreislauf mit Elektronen vollgestopft werden kann. Die Ursache hierfür liegt an der UV-Strahlung, vor allem in den Tagen vor der Ozonschicht, als mehr ultraviolette Strahlung bis zum Meeresspiegel vordrang. Ultraviolette Strahlen spalten nicht nur Wasser, sondern können auch Elektronen aus den in den Ozeanen gelösten Metallen und Mineralien herauslösen, allen voran Mangan und Eisen. Damit kommt ein Rinnsal von Elektronen kommt in den Kreislauf. Weder Eisen noch Mangan sind heute in hoher Konzentration im Meerwasser zu finden, denn die Ozeane sind durch und durch oxidiert; aber im Archaikum waren beide reichlich vorhanden. Mangan beispielsweise findet sich in großen Mengen auf dem Meeresboden in Form von merkwürdigen kegelförmigen „Knollen“, die sich im Laufe von Millionen von Jahren ansammeln. Man schätzt, dass eine Billion Tonnen manganhaltiger Knollen über den Meeresboden verstreut sind – eine riesige, aber unwirtschaftliche Reserve. Selbst die wirtschaftlicheren Reserven, wie die riesigen Kalahari-Manganfelder in Südafrika (weitere 13,5 Milliarden Tonnen Erz), wurden vor 2.400 Millionen Jahren aus den Ozeanen herausgeschwemmt. Kurz gesagt, die Ozeane waren einst voll von Mangan. Für Bakterien ist Mangan ein wertvolles Gut: Es wirkt als Antioxidans, das die Zellen vor der zerstörerischen Kraft der ultravioletten Strahlung schützt. Wenn ein Manganatom ein Photon der ultravioletten Strahlung absorbiert, gibt es ein Elektron ab, wird photooxidiert und „neutralisiert“ so die Strahlung. Das Mangan wird anstelle wichtigerer Teile der Zelle wie Proteine und DNA „geopfert“, die andernfalls von den Strahlen zerfetzt würden; und so nehmen Bakterien Mangan mit offenen Armen in ihre Behausung auf. Das Problem ist nur, dass diese Manganatome, wenn sie ein Elektron abgeben, immer vom Chlorophyll im Photosystem II verschluckt werden. Und so verstopft der Kreislauf allmählich mit Elektronen. Wenn es keine Möglichkeit gibt, die überschüssigen Elektronen, die den Kreislauf verstopfen, abzulassen, wird das Photosystem II immer weniger effizient.
Wie könnten Bakterien Elektronen aus dem Photosystem II abziehen? In unserem Fall wäre Photosystem II mit Elektronen verstopft, während Photosystem I untätig bleibt. Die Bakterien müssten nur den genetischen Schalter umlegen, dass beide Photosysteme gleichzeitig aktiv sind. So können die Elektronen von Photosystem II zum Photosystem I gelangen. Während die Elektronen von Photosystem II zu Photosystem I transportiert werden, kann die freigesetzte Energie zur Erzeugung von ATP genutzt werden. Bei Photosystem I angekommen werden die Elektronen durch das vom Licht angeregte Chlorophyll auf ein höheres Energieniveau gebracht und zum CO2 weitergegeben, um neue organische Stoffe herzustellen. Und das ist das eigentliche Z-Schema, das schon beschrieben wurde. Was eben noch als enorm komplizierter und aufwändiger Prozess erschien, wird plötzlich durch eine einzige Mutation praktisch unausweichlich.
Es lohnt sich, kurz zu rekapitulieren, um das Gesamtbild in seiner ganzen Tragweite zu erfassen. Am Anfang gab es ein einziges Photosystem, das wahrscheinlich das Sonnenlicht nutzte, um Elektronen aus Schwefelwasserstoff zu gewinnen und sie an Kohlendioxid abzugeben, um Zucker zu bilden. Irgendwann wurde das Gen dupliziert, vielleicht in einem Vorläufer der Cyanobakterien. Die beiden Photosysteme entwickelten sich unter unterschiedlicher Nutzung auseinander. Photosystem I machte genau das, was es vorher gemacht hatte, während Photosystem II sich darauf spezialisierte, ATP aus Sonnenlicht über einen Elektronenkreislauf zu erzeugen. Die beiden Photosysteme wurden je nach Umgebung ein- und ausgeschaltet, aber sie waren nie gleichzeitig eingeschaltet. Im Laufe der Zeit hat das Photosystem II jedoch ein Problem, das sich aus den Eigenschaften eines Elektronenkreislaufs ergibt: Jede zusätzliche Zufuhr von Elektronen aus der Umgebung stört den Kreislauf. Wahrscheinlich gab es eine ständige langsame Zufuhr von Elektronen aus Manganatomen, die von den Bakterien zum Schutz vor ultravioletter Strahlung verwendet werden. Eine Lösung bestand darin, den Schalter zu inaktivieren und beide Photosysteme gleichzeitig zu aktivieren. Die Elektronen würden dann von Mangan über beide Photosysteme zu Kohlendioxid fließen.
Ursprung des Wasserstoffspaltenden Komplexes
Wir sind jetzt nur noch einen Schritt von der vollwertigen sauerstoffhaltigen Photosynthese entfernt. Wir ziehen die Elektronen aus Mangan, nicht aus Wasser. Wie kam es also zu diesem endgültigen Wandel (siehe Cardona et al. 2015, Russel et al. 2008, Sauer & Yachandra 2002, Yano et al. 2006, Kuntzleman & Yocum 2005, Jablonsky & Lazar 2008, Renger 2012)? Die überraschende Antwort ist, dass sich praktisch nichts ändern musste. Der sauerstoffproduzierende Komplex ist der Nussknacker, der Wasser einfach so fesselt, um ihm seine Elektronen zu entreißen. Wenn alle Elektronen entfernt sind, wird der unschätzbare Abfall, der Sauerstoff, in die Welt hinausgespült. Der sauerstoffproduzierende Komplex ist eigentlich ein Bestandteil des Photosystems II, sitzt aber ganz am Rand, der Außenwelt zugewandt, und vermittelt den Eindruck, als sei er „angeheftet“. Er ist schockierend klein. Der Komplex besteht aus einem Cluster von vier Manganatomen und einem einzigen Kalziumatom, die alle von einem Gitter aus Sauerstoffatomen zusammengehalten werden.
Eine Forschergruppe in Berkely konnte die Struktur des sauerstoffproduzierenden Komplexes mittels Rüntgenkristallographie entschlüsseln und diese zeigt Ähnlichkeit mit dem Mineral Hollandit, welches u. a. in hydrothermalen Schloten entsteht.
Ob der ursprüngliche sauerstoffproduzierende Komplex einfach nur ein Stück Mineral war, das sich im Photosystem II verkeilt hat, wissen wir nicht. Vielleicht haben sich die Manganatome bei der Oxidation durch ultraviolette Strahlung mit dem Sauerstoff in einem Gitter verbunden und so das Wachstum eines winzigen Kristalls an Ort und Stelle ausgelöst. Vielleicht hat die Nähe dieses Clusters zum Chlorophyll oder zu benachbarten Proteinstücken ihn in irgendeiner Weise verzerrt und seine Funktion optimiert. Wie einige andere Metallcluster, die im Herzen von Enzymen gefunden wurden, ist es mit ziemlicher Sicherheit ein Rückfall in die Bedingungen, die vor Milliarden von Jahren in einem hydrothermalen Schlot herrschten. Das kostbarste aller Juwelen, das Metallcluster, war in ein Protein eingewickelt und wurde von den Cyanobakterien für alle Ewigkeit verwahrt.
Wie auch immer es entstanden ist, dieses kleine Bündel von Manganatomen eröffnete eine neue Welt, nicht nur für die Bakterien, die es zuerst einfingen, sondern für alles Leben auf unserem Planeten. Sobald es sich gebildet hatte, begann dieses kleine Atomcluster, Wasser zu spalten, wobei die vier oxidierten Manganatome ihre natürliche Neigung, dem Wasser Elektronen zu entziehen, kombinierten und dabei Sauerstoff als Abfallprodukt freisetzten. Angeregt durch die ständige Oxidation von Mangan durch ultraviolette Strahlung, verlief die Wasserspaltung zunächst nur langsam. Aber sobald der Cluster an das Chlorophyll gekoppelt war, begannen die Elektronen zu fließen. Je schneller sich das Chlorophyll an seine Aufgabe anpasste, desto mehr Wasser wurde angesaugt, aufgespalten, die Elektronen herausgezogen und der Sauerstoff entsorgt. Einst ein Rinnsal, schließlich eine Flut, ist dieser lebensspendende Elektronenfluss aus dem Wasser der Grund für die ganze Fülle des Lebens auf der Erde. Wir müssen ihm zweimal danken – einmal dafür, dass es die ultimative Quelle für all unsere Nahrung ist, und dann noch einmal für den Sauerstoff, den wir brauchen, um diese Nahrung zu verbrennen, um am Leben zu bleiben. Sie ist auch der Schlüssel zur Lösung der weltweiten Energiekrise. Wir brauchen nur die beiden aus dem Wasser freigesetzten Produkte: Sauerstoff und Wasserstoff. Wenn wir sie wieder miteinander reagieren lassen, erhalten wir die gesamte Energie, die wir jemals brauchen werden, und die einzige Verschwendung ist Wasser. Mit anderen Worten: Mit diesem kleinen Manganhaufen können wir die Energie der Sonne nutzen, um Wasser zu spalten und die Produkte dann wieder zusammenzufügen, um Wasser zu regenerieren – die Wasserstoffwirtschaft. Keine Umweltverschmutzung mehr, keine fossilen Brennstoffe, kein CO2-Fußabdruck, keine vom Menschen verursachte globale Erwärmung, wenn auch immer noch eine gewisse Explosionsgefahr. Wenn diese kleine Ansammlung von Atomen vor langer Zeit den Aufbau der Welt verändert hat, sollte die Kenntnis ihrer Struktur der erste Schritt sein, um unsere eigene Welt heute zu verändern.
Literatur
Alberts, B.; et al. (2024): Molekularbiologie der Zelle. New York: John Wiley & Sons.
Allen JF. (2005): A redox switch hypothesis for the origin of two light reactions in photosynthesis. FEBS Lett. 579(5):963-8.
Allen, J., Martin, W. (2007): Evolutionary biology – Out of thin air. Nature 445: 610-2.
Blankenship RE (2014): Molecular Mechanisms of Photosynthesis (2nd ed.).
Blankenship, R.E., Madigan, M.T., Bauer, C.E. (2006): Anoxygenic Photosynthetic Bacteria
Bryant DA, Costas AM, Maresca JA, Chew AG, Klatt CG, Bateson MM, Tallon LJ, Hostetler J, Nelson WC, Heidelberg JF, Ward DM (2007): Candidatus Chloracidobacterium thermophilum: An Aerobic Phototrophic Acidobacterium. Science. 317 (5837): 523–6.
Bryant D. A.; Frigaard, N.-U. (2006): Prokaryotic photosynthesis and phototrophy illuminated. Trends in Microbiology. 14 (11): 488–496
Campbell, N. A. et al. (2016): Biologie. München: Pearson.
Cardona T. (2015): A fresh look at the evolution and diversification of photochemical reaction centers. Photosynthesis Research 126: 111–134.
Cardona T. (2017): Photosystem II is a chimera of reaction centers. Journal of Molecular Evolution 84: 149–151.
Cardona T. (2018): Early Archean origin of heterodimeric Photosystem I. Heliyon 4: e00548.
Cardona T. (2019): Thinking twice about the evolution of photosynthesis. Open Biol. 9(3): 180246.
Cardona T, Murray JW, Rutherford AW. (2015): Origin and evolution of water oxidation before the last common ancestor of the Cyanobacteria. Molecular Biology and Evolution 32: 1310–1328.
Cardona T, Rutherford AW. (2019): Evolution of photochemical reaction centres: more twists? Trends in Plant Science 24: 1008–1021.
Cardona T, Sánchez-Baracaldo P, Rutherford AW, Larkum AWD. (2019): Early Archean origin of Photosystem II. Geobiology 17: 127–150.
Cox, N.; Pantazis, D. A.; Lubitz, W. (2020): Current Understanding of the Mechanism of Water Oxidation in Photosystem II and Its Relation to XFEL Data. Annual Review of Biochemistry 89: 795–820.
Ferreira KN, Iverson TM, Maghlaoui K, Barber J, Iwata S (2004): Architecture of the photosynthetic oxygen-evolving center. Science. 303 (5665): 1831–8.
Golbeck JH (1987): Structure, function and organization of the Photosystem I reaction center complex. Biochimica et Biophysica Acta (BBA) – Reviews on Bioenergetics. 895 (3): 167–204.
Gould, S. B., Waller, R. F., McFadden, G. I. (2008): Plastid Evolution. Annual Review of Plant Biology 59, S. 491–517.
Guskov A, Kern J, Gabdulkhakov A, Broser M, Zouni A, Saenger W (2009): Cyanobacterial photosystem II at 2.9-A resolution and the role of quinones, lipids, channels and chloride. Nature Structural & Molecular Biology. 16 (3): 334–42.
Hill, R. (1937): Oxygen Evolved by Isolated Chloroplasts. Nature. 139 (3525): 881–882.
Hill, R. (1939): Oxygen Produced by Isolated Chloroplasts. Proceedings of the Royal Society B: Biological Sciences. 127 (847): 192–210.
Hill, R.; Bendall, F. (1960): Function of the Two Cytochrome Components in Chloroplasts: A Working Hypothesis. Nature. 186 (4719): 136–137.
Hill, R.; Scarisbrick, R. (1940): Production of Oxygen by Illuminated Chloroplasts. Nature. 146 (3689): 61–62.
Hill, R.; Whittingham, C.P. (1953): Photosynthesis. London: Methuen.
Hohmann-Marriott MF, Blankenship RE. (2011): Evolution of photosynthesis. Annual Review of Plant Biology 62: 515–548.
Hope AB (2000): Electron transfers amongst cytochrome f, plastocyanin and photosystem I: kinetics and mechanisms. Biochimica et Biophysica Acta (BBA) – Bioenergetics. 1456(1), 5–26.
Jablonsky J, Lazar D (2008): Evidence for intermediate S-states as initial phase in the process of oxygen-evolving complex oxidation. Biophysical Journal. 94 (7): 2725–36.
Kuntzleman T, Yocum CF (2005): Reduction-induced inhibition and Mn(II) release from the photosystem II oxygen-evolving complex by hydroquinone or NH2OH are consistent with a Mn(III)/Mn(III)/Mn(IV)/Mn(IV) oxidation state for the dark-adapted enzyme. Biochemistry. 44 (6): 2129–42.
Lockau W, Nitschke W (1993): Photosystem I and its Bacterial Counterparts. Physiologia Plantarum. 88 (2): 372–381.
Loll B, Kern J, Saenger W, Zouni A, Biesiadka J (2005): Towards complete cofactor arrangement in the 3.0 A resolution structure of photosystem II. Nature. 438(7070): 1040–4.
Madigan, M. T.; et al. (2020): Brock Mikrobiologie. München: Pearson.
Margulis (Sagan), L (1967): On the Origin of Mitosing Cells. Journal of Theoretical Biology. 14 (3): 225–274.
Margulis, L. (1970): Origin of Eukaryotic Cells, Yale University Press
Margulis, L; Bermudes, D (1985): Symbiosis as a mechanism of evolution: status of cell symbiosis theory. Symbiosis. 1: 101–124.
Margulis, L., Sagan, D. (1997): Leben: Vom Ursprung zur Vielfalt. Spektrum Akademischer Verlag, Heidelberg/Berlin
Martin, W. F., Garg, S., Zimorski, V. (2015): Endosymbiotic theories for eukaryote origin. Philosophical Transactions of the Royal Society of London B: Biological Sciences 370(1678)
Martin, W. F., Bryant, D., Beatty, J. (2017): A physiological perspective on the origin and evolution of photosynthesis. FEMS microbiology reviews 42.
Mauzerall DC (1998): Evolution of porphyrins. Clin Dermatol 16(2):195-201.
McFadden, G. I. (2001): Primary and secondary endosymbiosis and the origin of plastids. Journal of Phycology 37, S. 951–959.
Mulkidjanian AY, Koonin EV, Makarova KS, Mekhedov SL, Sorokin A, Wolf YI, Dufresne A, Partensky F, Burd H, Kaznadzey D et al. (2006): The cyanobacterial genome core and the origin of photosynthesis. Proceedings of the National Academy of Sciences, USA 103: 13126–13131.
Munk, K. (2008): Taschenlehrbuch Biologie: Botanik. Stuttgart: Georg Thieme Verlag.
Munk, K. (2018): Taschenlehrbuch Biologie: Mikrobiologie. Stuttgart: Georg Thieme Verlag.
Nelson, D.; Cox, M. (2010): Lehninger Biochemie. Wiesbaden: Springer Berlin Heidelberg.
Nelson N, Yocum CF (2006): Structure and function of photosystems I and II. Annual Review of Plant Biology. 57: 521–65.
Okubo T, Tomo T, Sugiura M, Noguchi T (2007): Perturbation of the structure of P680 and the charge distribution on its radical cation in isolated reaction center complexes of photosystem II as revealed by fourier transform infrared spectroscopy. Biochemistry. 46 (14): 4390–7
Oliver T, Kim TD, Trinugroho JP, Cordón-Preciado V, Wijayatilake N, Bhatia A, Rutherford AW, Cardona T. (2023): The Evolution and Evolvability of Photosystem II. Annu Rev Plant Biol. 22(74):225-257.
Orf GS, Gisriel C, Redding KE (2018): Evolution of photosynthetic reaction centers: insights from the structure of the heliobacterial reaction center. Photosynthesis Research 138(1): 11–37
Raymond J, Zhaxybayeva O, Gogarten JP, Gerdes SY, Blankenship RE. (2002): Whole-genome analysis of photosynthetic prokaryotes. Science 298: 1616–1620.
Renger G (2012): Mechanism of light induced water splitting in Photosystem II of oxygen evolving photosynthetic organisms. Biochimica et Biophysica Acta (BBA) – Bioenergetics. 1817 (8): 1164–76.
Russell, M, Allen, J., Milner-White, E. (2008): Inorganic Complexes Enabled the Onset of Life and Oxygenic Photosynthesis. 10.1007/978-1-4020-6709-9_259.
Rutherford AW, Faller P (2003): Photosystem II: evolutionary perspectives. Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences 358 (1429): 245–53.
Rutherford AW, Heathcote P (1985): Primary photochemistry in photosystem-I. Photosynthesis Research. 6 (4): 295–316.
Sadava, D., et al. (2019): Purves Biologie. Berlin Heidelberg New York: Springer-Verlag.
Sadekar S, Raymond J, Blankenship RE (2006): Conservation of distantly related membrane proteins: photosynthetic reaction centers share a common structural core. Molecular Biology and Evolution. 23 (11): 2001–7.
Sánchez-Baracaldo P, Cardona T. (2019): On the origin of oxygenic photosynthesis and Cyanobacteria. New Phytol. 225(4):1440-1446.
Sauer K, Yachandra VK. (2002): A possible evolutionary origin for the Mn4 cluster of the photosynthetic water oxidation complex from natural MnO2 precipitates in the early ocean. Proc Natl Acad Sci U S A. 99(13):8631-6.
Shubin VV, Karapetyan NV, Krasnovsky AA (1986): Molecular arrangement of pigment-protein complex of photosystem 1. Photosynthesis Research. 9 (1–2): 3–12.
Soo RM, Hemp J, Parks DH, Fischer WW, Hugenholtz P. (2017): On the origins of oxygenic photosynthesis and aerobic respiration in Cyanobacteria. Science 355: 1436–1440.
Turner, S. et al. (1999): Investigating deep phylogenetic relationships among Cyanobacteria and plastids by small subunit rRNA sequence analysis. Journal of Eukaryotic Microbiology 46, S. 327–338.
Walker, D. A. (2002a): ‚And whose bright presence‘ – an appreciation of Robert Hill and his reaction. Photosynthesis Research. 73 (1/3): 51–54
Walker, D. A. (2002b): The Z-scheme – down hill all the way. Trends in Plant Science. 7 (4): 183–185.
Walker, D. A.; Hill, R (1967): The relation of oxygen evolution to carbon assimilation with isolated chloroplasts. Biochimica et Biophysica Acta (BBA) – Bioenergetics. 131 (2): 330–8.
Weiler, E. W. et al. (2008): Allgemeine und molekulare Botanik. Stuttgart: Thieme.
Yamori W, Shikanai T (2016): Physiological Functions of Cyclic Electron Transport Around Photosystem I in Sustaining Photosynthesis and Plant Growth. Annual Review of Plant Biology 67: 81–106.
Yano J, Kern J, Sauer K, Latimer MJ, Pushkar Y, Biesiadka J, Loll B, Saenger W, Messinger J, Zouni A, Yachandra VK (2006): Where water is oxidized to dioxygen: structure of the photosynthetic Mn4Ca cluster. Science 314(5800):821-5.
Zouni A, Witt HT, Kern J, Fromme P, Krauss N, Saenger W, Orth P (2001): Crystal structure of photosystem II from Synechococcus elongatus at 3.8 A resolution. Nature 409(6821): 739–43.